Перейти к:
Особенности клинико-лабораторных показателей у больных с хронической сердечной недостаточностью пожилого и старческого возраста при дефиците железа
https://doi.org/10.37489/2949-1924-0004
Аннотация
Актуальность. Частота хронической сердечной недостаточности (ХСН) увеличивается с возрастом. Распространённой патологией у больных с ХСН является дефицит железа (ДЖ). Развитию ДЖ у больных с ХСН может способствовать возраст. Цель исследования: сопоставить особенности клинических и лабораторных показателей у пациентов с ХСН пожилого и старческого возраста в зависимости от наличия ДЖ. Материалы и методы: обследовано 2 группы больных с ХСН 2-4-го функционального класса: 1-я группа — 60-74 года (146 больных, средний возраст 68,1±3,1), 2-я группа — 75 лет и старше (127 пациентов, средний возраст 78,3±2,2). У всех больных проводили клиническое обследование, тест 6-минутной ходьбы, общий анализ крови, определение в сыворотке крови уровня железа, ферритина, трансферрина, насыщения трансферрина железом, растворимых рецепторов трансферрина, гепсидина, интерлейкина-6, С-реактивного белка, наличия и выраженности астении, тревоги, депрессии. Результаты. Установлено, что больные старческой группы имеют достоверно большую выраженность латентного ДЖ и более выраженные клинико-лабораторные проявления ХСН (меньшую дистанцию теста 6-минутной ходьбы, более выраженные проявления астении и депрессии, большую концентрацию NT-proBNP, гепсидина), по сравнению с пожилыми больными. Наличие ДЖ в обеих возрастных группах усиливает проявления физической астении и тревоги. Выводы: 1) выраженность клинических проявлений ХСН у больных старческого возраста достоверно больше, чем у пожилых пациентов; 2) у больных старческого возраста достоверно выше, чем у пожилых пациентов, уровень гепсидина и выраженность латентного ДЖ; 3) латентный ДЖ в обеих возрастных группах усиливает проявления физической астении и тревоги; 4) целесообразно проведение ранней диагностики латентного ДЖ у всех больных с ХСН пожилого и особенно старческого возраста для своевременного выявления данного состояния и назначения терапии для коррекции ДЖ.
Для цитирования:
Смирнова М.П., Чижов П.А., Корсакова Д.А., Баранов А.А. Особенности клинико-лабораторных показателей у больных с хронической сердечной недостаточностью пожилого и старческого возраста при дефиците железа. Пациентоориентированная медицина и фармация. 2023;1(1):23-31. https://doi.org/10.37489/2949-1924-0004
For citation:
Smirnova M.P., Chizhov P.A., Korsakova D.A., Baranov A.A. Characteristics of clinical and laboratory parameters in patients with chronic heart failure of elderly and senile age with iron deficiency. Patient-Oriented Medicine and Pharmacy. 2023;1(1):23-31. (In Russ.) https://doi.org/10.37489/2949-1924-0004
Введение / Introduction
Хроническая сердечная недостаточность (ХСН) — частое осложнение большинства сердечно-сосудистых заболеваний. Распространённость ХСН увеличивается с возрастом: примерно с 1 % для лиц в возрасте <55 лет до >10 % для лиц в возрасте 70 лет и старше [1]. Более 65 % больных ХСН находятся в возрастных группах старше 60 лет [2].
Распространённым коморбидным состоянием у больных с ХСН является дефицит железа (ДЖ), который выявляется у 34-83 % пациентов с ХСН [3-6]. ДЖ значительно снижает функциональную активность и качество жизни больных ХСН, увеличивает частоту госпитализаций и смертность [5][7][8]. Коррекция ДЖ у больных с ХСН улучшает функциональные способности больных и качество их жизни и снижает число повторных госпитализаций [7-9].
Одним из факторов, способствующих развитию ДЖ у больных с ХСН, может быть возраст [8][10][11].
Учитывая нарастание распространённости ХСН в старших возрастных группах и увеличение средней продолжительности жизни населения России, а также потенциально негативную роль возраста для развития ДЖ, представляет интерес исследование клинических особенностей и лабораторных показателей, характеризующих обмен железа у пациентов с ХСН пожилого и старческого возраста. Ранее подобное комплексное исследование клинико-лабораторных показателей у больных с ХСН старших возрастных групп не проводилось.
Цель исследования / The purpose of the study
Сопоставить клинические и лабораторные показатели у пациентов с хронической сердечной недостаточностью пожилого и старческого возраста и изучить их особенности в зависимости от наличия дефицита железа.
Материалы и методы / Materials and methods
Обследовано 273 больных (67 мужчин и 206 женщин) с ХСН разного функционального класса (средний возраст 71,3±8,1 года), находившихся на лечении в терапевтическом отделении больницы № 1 г. Ярославля по поводу ухудшения течения ИБС и / или гипертонической болезни и нарастания симптомов ХСН. Все обследованные были разделены на 2 группы: 1-я группа — 60-74 года (146 больных, средний возраст 68,1±3,1, 45 мужчин и 101 женщина), 2-я группа — 75 лет и старше (127 пациентов; средний возраст 78,3±2,2; 22 мужчины и 105 женщин). В 1-й группе 2-го ФК (NYHA) ХСН имели 70 больных (48 % от данной группы), 3-го ФК — 55 (38 %), 4-го ФК — 21 (14 %). Во второй группе 2-го ФК ХСН имели 22 (17 %) больных, 3-го ФК — 82 (65 %), 4-го ФК — 23 (18 %).
У всех больных проводили клиническое обследование с расчётом баллов по шкале оценки клинического состояния больных с ХСН (ШОКС), тест 6-минутной ходьбы (Т6М), определяли наличие и выраженность астении по шкале MFI-20 и тревоги и депрессии по госпитальной шкале тревоги и депрессии (HADS). У всех больных проводили общий анализ крови на гематологическом анализаторе MEK 6500 (Япония) с определением количества эритроцитов (RBC) x1012 / л, уровня гемоглобина (HGB) в г / л, гематокрита (HCT) в процентах, среднего объёма эритроцита (MCV) во фл, среднего содержания (MCH) в пг и средней концентрации гемоглобина в эритроците (MCHC) в г / л, распределения эритроцитов по объёму (RDW) в процентах. Кроме того, исследовали на медицинском лабораторном фотометре (ИФА-ридере) Immunochem-2100 методом иммуноферментного анализа уровень NT-концевого предшественника мозгового натрийуретического пептида (NT-proBNP) в пг / мл, гепсидина в нг / мл, интерлейкина-6 в пг / мл, растворимых рецепторов трансферрина (РРТР) в нмоль / л. Концентрацию железа в мкмоль / л, трансферрина в г / л, ферритина в мкг / л, С-реактивного белка (СРБ) в мг / л в сыворотке крови определяли на гематологическом анализаторе SAPPHIRE-400 (Япония) фотометрическим методом по конечной точке; коэффициент насыщения трансферрина железом (КНТЖ) в процентах рассчитывали по формуле: железо сыворотки, мкмоль / л х 398 / трансферрин, мг / дл.
О наличии дефицита железа судили в соответствии с клиническими рекомендациями ОССН-РКО-РНМОТ 2018 [2] на основании снижения уровня ферритина сыворотки крови менее 100 мкг / л или ферритина в диапазоне от 100 до 299 мкг / л и насыщения трансферрина железом менее 20 %. Всем больным регистрировали ЭКГ и проводили эхокардиографию на аппарате экспертного класса GE WIWID-7.
Статистический анализ полученных результатов проводился с помощью программы Statistica 10.0. Нормальность распределения выборки оценивали тестом Шапиро — Уилка. При нормальном распределении для сравнения средних значений двух выборок использовали t-критерий Стьюдента. Данные представлены в виде среднего (М) и стандартного отклонения (SD). При распределении, отличном от нормального, для сравнения результатов в двух группах применяли U-тест Манна — Уитни. Данные представлены в виде медианы (Ме) и 25-го и 75-го перцентилей. Для оценки наличия связи между разными параметрами рассчитывали коэффициент ранговой корреляции Спирмена. За уровень достоверности принят p <0,05.
Результаты и обсуждение / Results and discussion
Сопоставление изученных показателей у больных разного возраста по группам в целом показало, что у пациентов старшей возрастной группы достоверно меньше дистанция Т6М и больше ШОКС, выраженность депрессии и астении по шкалам общей и физической астении, пониженной активности и снижения мотивации, а также суммарной астении. Кроме того, в группе больных 75 лет и старше достоверно ниже число эритроцитов, уровень гемоглобина, гематокрита, концентрация ферритина и выше уровень гепсидина и NT-proBNP (табл. 1). Достоверной разницы в содержании железа в крови у пациентов этих групп не выявлено.
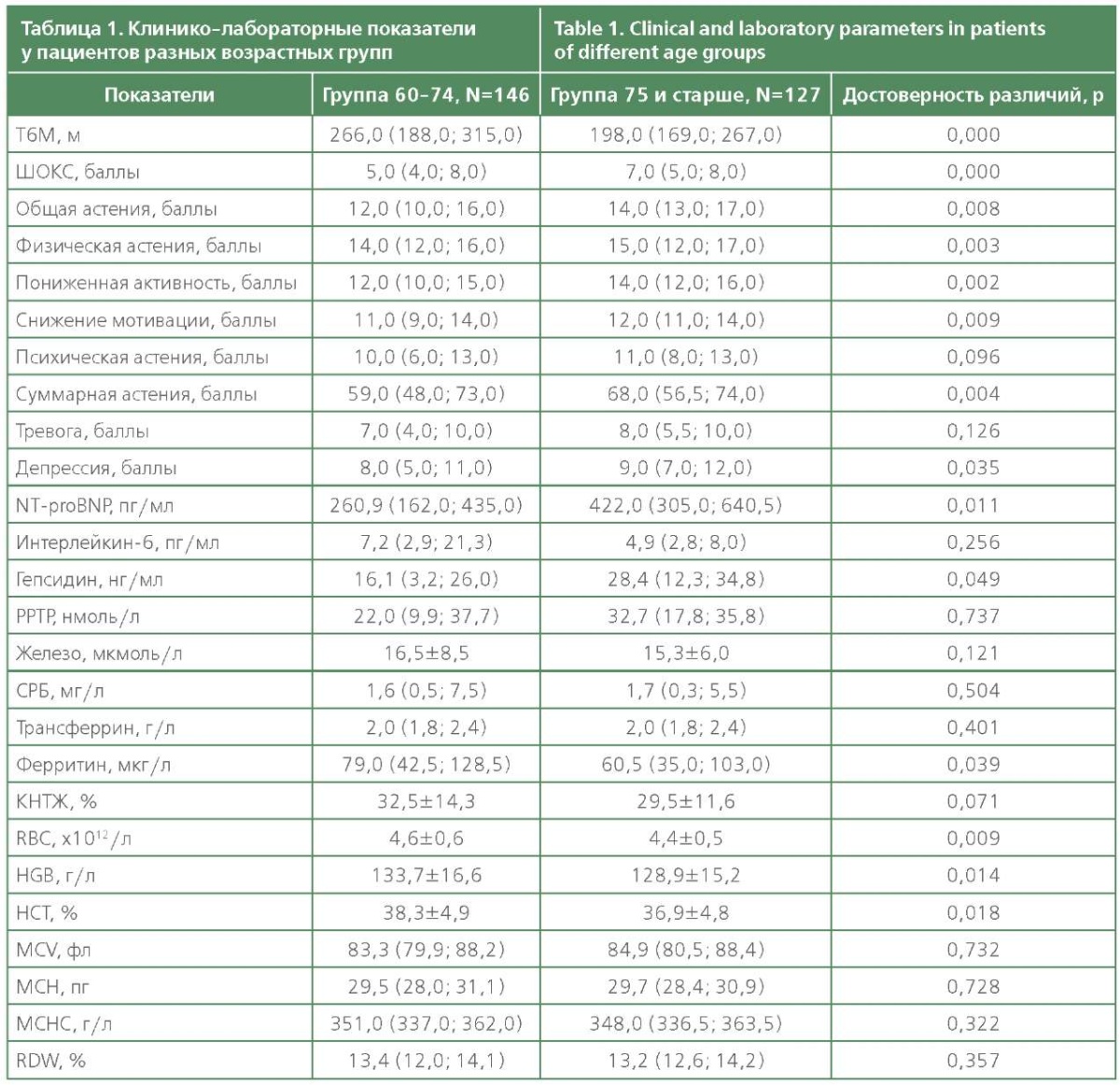
По группе в целом получены достоверные положительные корреляции средней силы между возрастом и ШОКС (0,42), всеми показателями астении (0,32-0,41), тревоги (0,33) и депрессии (0,43), уровнем гепсидина (0,38) и NT-proBNP (0,36), а также достоверные отрицательные корреляции средней силы между возрастом и Т6М ( — 0,34), уровнем ферритина ( — 0,32), гемоглобина ( — 0,38), количеством эритроцитов ( — 0,33) и гематокритом ( — 0,32).
ДЖ выявлен у 195 (71 %) обследованных; частота ДЖ не имела отличий в сравниваемых подгруппах — 70 % в 1-й группе и 73 % — во второй.
В табл. 2 представлены значения исследуемых показателей у пациентов с ХСН в возрасте 60-74 года в зависимости от наличия ДЖ.
Как видно из данных, представленных в табл. 2, у пожилых пациентов при наличии ДЖ достоверно больше выраженность физической астении и тревоги. Кроме того, у больных с ДЖ достоверно выше уровень интерлейкина-6 и гепсидина и ниже уровень железа, гемоглобина, гематокрит и MCH, по сравнению с пациентами без ДЖ.

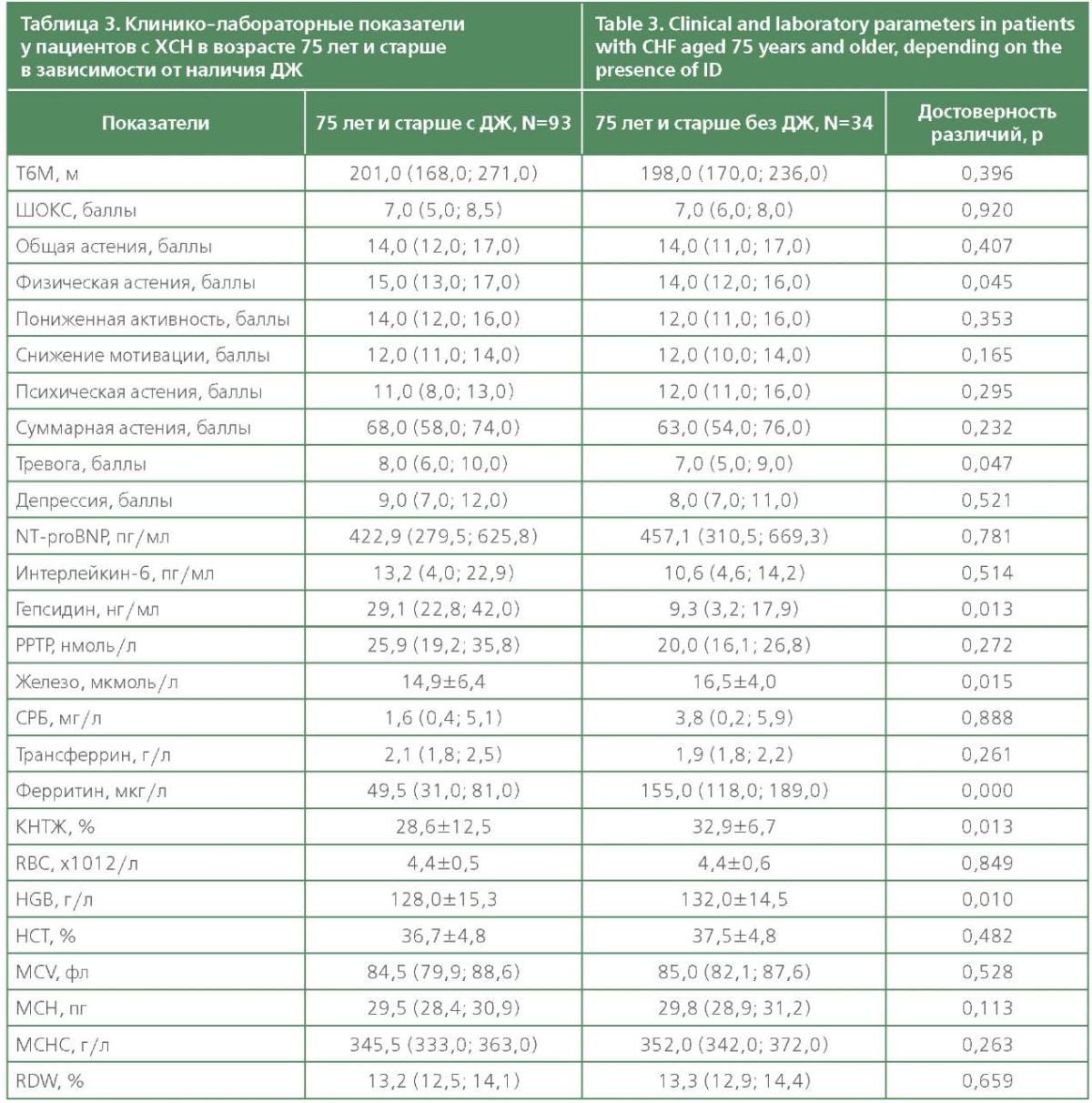
С целью оценки влияния ДЖ на исследуемые клинические и лабораторные показатели в старшей возрастной группе проведено их сопоставление в подгруппах в зависимости от наличия ДЖ, результаты представлены в табл. 3.
Как видно из данных, представленных в табл. 3, у обследованных старшей возрастной группы с ДЖ также достоверно ниже уровень железа, гемоглобина и гематокрит и достоверно выше выраженность физической астении и тревоги, по сравнению с обследованными без ДЖ.
Обсуждение / Discussion
Проведённое исследование показало, что больные старшей возрастной группы (75 лет и старше) имеют существенные достоверные отличия клинико-лабораторных показателей от таковых у пациентов 60-74 лет. В частности, у них достоверно ниже функциональная активность по Т6М и более выражены клинико-лабораторные проявления ХСН (баллы ШОКС, различные проявления астении, депрессия, уровень NT-proBNP). Кроме того, у пациентов старшей возрастной группы установлено меньшее число эритроцитов и более низкие уровни гемоглобина и гематокрита. Особое внимание обращает на себя концентрация ферритина в крови обследованных пациентов. В обеих группах больных средняя по группам концентрация ферритина ниже 100 мкг / л. Это свидетельствует о снижении запасов железа в организме у пациентов обеих групп. Однако в старшей возрастной группе уровень ферритина достоверно ниже, чем у больных 60-74 лет, и, следовательно, выраженность латентного дефицита железа выше.
Таким образом, старческий возраст у больных с ХСН способствует развитию достоверно большего латентного ДЖ, по сравнению с пожилыми больными, и существенно ухудшает клинические проявления ХСН.
Одним из механизмов, ведущих к развитию латентного ДЖ, может быть накопление железа макрофагами под влиянием увеличенной продукции гепсидина вследствие системного воспаления [11-13]. Возможное участие данного механизма шей группы подтверждают и результаты нашей работы: у больных 75 лет и старше уровень гепсидина был достоверно выше, чем у пациентов 60-74 лет.
Более выраженный латентный ДЖ может быть одной из причин утяжеления функциональных нарушений в старшей возрастной группе. Железо входит в состав многих окислительно-восстановительных ферментов кардиомиоцитов и скелетных мышц [14][15]. Поэтому при снижении запасов железа в организме нарушается энергетический метаболизм кардиомиоцитов [16] и скелетных мышц [17] и снижается функциональная способность больных, что и проявляется снижением Т6М, нарастанием различных проявлений астении и повышением ШОКС. Ранее показано, что содержание железа в миокарде больных с тяжёлой сердечной недостаточностью снижено на 20-30 % [18].
Ещё одним фактором, определяющим большее снижение функциональных способностей пациентов в старшей возрастной группе, может быть меньший уровень гемоглобина у них, что тоже может быть в какой-то мере обусловлено ДЖ.
Большая выраженность депрессии у больных старшей возрастной группы также может определяться более выраженным ДЖ у этих пациентов. Это обусловлено тем, что железо необходимо для функционирования таких ферментов, как тирозингидроксилаза и триптофангидроксилаза, которые требуются для синтеза дофамина и серотонина. Дефицит последних способствует развитию депрессии [19][20].
Значение возраста для тяжести клинических проявлений ХСН и выраженности лабораторных изменений подтверждают установленные положительные корреляции между возрастом и ШОКС, всеми показателями астении, тревоги и депрессии, уровнем гепсидина и NT-proBNP, а также достоверные отрицательные корреляции между возрастом и Т6М, уровнем ферритина, гемоглобина, количеством эритроцитов и гематокритом.
Сопоставление исследованных показателей в подгруппах больных с наличием и отсутствием ДЖ в обеих исследованных возрастных группах подтверждает значение функционального ДЖ как одной из причин нарастания клинических проявлений ХСН: при наличии ДЖ наблюдается усиление физической астении и тревоги. Следует отметить, что, хотя уровень железа и гемоглобина в среднем в подгруппах с наличием и отсутствием ДЖ в обеих возрастных группах находился в пределах нормы, у пациентов с ДЖ в обеих возрастных группах они были достоверно ниже, чем у больных без ДЖ. Это тоже в определённой степени может способствовать нарастанию астении.
Достоверное повышение содержания в крови интерлейкина-6 при наличии ДЖ у пациентов 60-74 лет подтверждает активацию системного воспаления у этих больных [11][12], следствием чего и является увеличение образования гепсидина [11][12]. У больных старческого возраста при наличии ДЖ достоверного повышения уровня интерлейкина-6 не установлено, однако концентрация гепсидина у этих пациентов была достоверно выше, чем при отсутствии ДЖ. Эти данные подтверждают важную роль системного воспаления и избыточной продукции гепсидина в механизме развития латентного ДЖ у больных с ХСН. В реальной клинической практике, исследования, позволяющие диагностировать латентный ДЖ у больных с ХСН, проводятся в единичных случаях.
Выводы / Findings
- Выраженность клинических проявлений ХСН (снижение функциональной активности, нарастание различных проявлений астении и депрессии) у больных 75 лет и старше достоверно больше, чем у пожилых пациентов.
- У больных с ХСН 75 лет и старше достоверно выше, чем у пациентов 60-74 лет, уровень гепсидина, выраженность латентного дефицита железа, а также ниже число эритроцитов и концентрация гемоглобина.
- Латентный дефицит железа в обеих исследованных возрастных группах усиливает проявления физической астении и тревоги.
- Целесообразно проведение ранней диагностики латентного дефицита железа у всех больных с ХСН пожилого и особенно старческого возраста для своевременного выявления данного состояния и назначения терапии для коррекции ДЖ.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Соответствие нормам этики.
Все участники исследования подписывали информированное согласие. Протокол исследования был одобрен этическим комитетом Федерального государственного бюджетного образовательного учреждения высшего образования «Ярославский государственный медицинский университет» МЗ РФ (протокол №м19 от 26.10.2017).
Конфликт интересов.
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
Благодарности.
Работа выполнялась без спонсорской поддержки.
Участие авторов.
Смирнова М. П. — обследование больных, сбор, обработка и анализ данных, изучение литературы по предмету исследования, написание статьи; Чижов П. А. — анализ и интерпретация результатов работы, критический пересмотр содержания текста рукописи, участие в редактировании текста рукописи; Корсакова Д. А. — обследование больных, сбор, обработка и анализ данных; Баранов А. А. — организация лабораторных обследований.
ADDITIONAL INFORMATION
Compliance with ethical standards.
All study participants signed an informed consent. The study protocol was approved by the Ethics Committee of the Federal State Budgetary Educational Institution of Higher Education «Yaroslavl State Medical University» of the Ministry of Health of the Russian Federation (protocol No. 19 dated October 26, 2017).
Conflict of interests.
Authors declare no conflict of interest requiring disclosure in this article.
Acknowledgments.
The work was carried out without sponsorship.
Participation of authors.
Smirnova MP — examination of patients, collection, processing and analysis of data, study of literature on the subject of research, writing an article; Chizhov PA — analysis and interpretation of the results of the work, critical revision of the content of the text of the manuscript, participation in editing the text of the manuscript; Korsakova DA — examination of patients, collection, processing and analysis of data; Baranov AA — organization of laboratory research.
Список литературы
1. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal. 2021;42:3599-726. doi: 10.1093/eurheartj/ehab368
2. Клинические рекомендации ОССН — РКО — РНМОТ. Сердечная недостаточность: хроническая (ХСН) и острая декомпенсированная (ОДСН). Диагностика, профилактика и лечение. Кардиология. 2018;58 (S6):8-164. doi: 10.18087/cardio.2475.
3. Kurz K, Lanser L, Seifert M et al. Anaemia, iron status, and gender predict the outcome in patients with chronic heart failure. ESC Heart Failure. 2020;7:1880-90. Published online 27 May 2020 in Wiley Online Library (wileyonlinelibrary.com). doi: 10.1002/ehf2.12755
4. Moliner P, Enjuanes C, Tajes M et al. Association between norepinephrine levels and abnormal iron status in patients with chronic heart failure: is iron deficiency more than a comorbidity? J Am Heart Assoc. 2019 Feb 19;8 (4):e010887. doi: 10.1161/JAHA.118.010887
5. Beattie JM, Khatib R, Phillips CJ, Williams SJ. Iron deficiency in 78 805 people admitted with heart failure across England: a retrospective cohort study. Open Heart. 2020 Mar 11;7 (1):e001153. doi: 10.1136/openhrt-2019-001153
6. von Haehling S, Ebner N, Evertz R et al. Iron deficiency in heart failure: an overview. JACC Heart Fail. 2019 Jan;7 (1):36-46. doi: 10.1016/j.jchf.2018.07.015
7. Jankowska EA, Tkaczyszyn M, Suchocki Tet al. Effects of intravenous iron therapy in irondeficient patients with systolic heart failure: a meta-analysis of randomized controlled trials. Eur J Heart Fail. 2016;18:786-95. doi: 10.1002/ejhf.473
8. Anker SD, Kirwan BA, van Veldhuisen DJ et al. Effects of ferric carboxymaltose on hospitalisations and mortality rates in iron-deficient heart failure patients: an individual patient data metaanalysis. Eur J Heart Fail. 2018;20:125-33. doi: 10.1002/ejhf.823
9. Смирнова М. П., Чижов П. А., Баранов А. А. Эффективность внутривенного введения железа (III) гидроксид сахарозного комплекса у пациентов с хронической сердечной недостаточностью с сохранённой фракцией выброса и дефицитом железа. Вестник современной клинической медицины. 2022;15 (5):66-72. doi: 10.20969/VSKM.2022.15(5).66-72.
10. Rizzo C, Carbonara R, Ruggieri R et al. Iron deficiency: a new target for patients with heart failure. Front Cardiovasc Med. 2021;8:709872. doi: 10.3389/fcvm.2021.709872
11. Соломахина Н. И., Находнова Е. С., Ершов В. И., Беленков Ю. Н. Роль гепсидина в формировании анемии хронических заболеваний и железодефицитной анемии у больных с хронической сердечной недостаточностью в пожилом и старческом возрасте. Кардиология. 2018;58 (3):20-7. doi: 10.18087/cardio.2018.3.10094.
12. Ватутин Н. Т., Тарадин Г. Г., Канишева И. В., Венжега В. В. Анемия и железодефицит у больных с хронической сердечной недостаточностью. Кардиология. 2019;59 (4S): 4-20. doi: 10.18087/cardio.2638.
13. Стуклов Н. И. Дефицит железа и анемия у больных хронической сердечной недостаточностью. Рациональная фармакотерапия в кардиологии. 2017;13 (5):651-60. doi: 10.20996/1819-6446-2017-13-5-651-660.
14. Galy B, Ferring-Appel D, Sauer SW et al. Iron regulatory proteins secure mitochondrial iron sufficiency and function. Cell Metab. 2010;12:194-201.
15. Hower V, Mendes P, Torti FM et al. A general map of iron metabolism and tissue-specific subnetworks. Mol Biosyst. 2009;5:422-43.
16. Hoes MF, Grote BN, Kijlstra JD et al. Iron deficiency impairs contractility of human cardiomyocytes through decreased mitochondrial function. Eur J Heart Fail. 2018;20:910-9. doi: 10.1002/ejhf.1154
17. Rizzo C, Carbonara R, Ruggieri R et al. Iron deficiency: a new target for patients with heart failure. Front Cardiovasc Med. 2021;8:709872. doi: 10.3389/fcvm.2021.709872
18. Maeder MT, Khammy O, Remrdios C, Kaye DM. Myocardial and systemic iron depletion in heart failure: implicatins for anemia accompanying heart failure. J Am Coll Cardiol. 2011;58 (5):474-80. doi: 10.1016/j.jacc.2011.01.059
19. Philip Saltiel PhF, Silverstein DI. Major depressive disorder: mechanism-based prescribing for personalized medicine. Neuripsychiatric Disease and Treatment. 2015;11:8750888. doi: 10.2147/NDT.S73261
20. Nnah IC, Wessling-Resnick M. Brain Iron Homeostasis: A Focus on microglial. Iron Pharmaceuticals (Basel). 2018;11 (4):129-55. doi: 10.3390/ph11040129
Об авторах
М. П. СмирноваРоссия
Смирнова Марина Петровна — к. м. н., доцент кафедры факультетской терапии
eLibrary SPIN-код: 4399-0900
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
П. А. Чижов
Россия
Чижов Пётр Александрович — д. м. н., проф., зав. кафедрой факультетской терапии
eLibrary SPIN-код: 6427-4298
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
Д. А. Корсакова
Россия
Корсакова Дарья Александровна — аспирант кафедры факультетской терапии
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
А. А. Баранов
Россия
Баранов Андрей Анатольевич — д. м. н., проф., зав. кафедрой поликлинической терапии, клинической лабораторной диагностики и медицинской биохимии
eLibrary SPIN-код: 4497-7008
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
Рецензия
Для цитирования:
Смирнова М.П., Чижов П.А., Корсакова Д.А., Баранов А.А. Особенности клинико-лабораторных показателей у больных с хронической сердечной недостаточностью пожилого и старческого возраста при дефиците железа. Пациентоориентированная медицина и фармация. 2023;1(1):23-31. https://doi.org/10.37489/2949-1924-0004
For citation:
Smirnova M.P., Chizhov P.A., Korsakova D.A., Baranov A.A. Characteristics of clinical and laboratory parameters in patients with chronic heart failure of elderly and senile age with iron deficiency. Patient-Oriented Medicine and Pharmacy. 2023;1(1):23-31. (In Russ.) https://doi.org/10.37489/2949-1924-0004


































.png)
