Перейти к:
Прогнозирование риска тромбоза постоянного сосудистого доступа
https://doi.org/10.37489/2949-1924-0020
Аннотация
Цель: улучшить результаты хирургического лечения пациентов со сформированными первичными артериовенозными фистулами. Материалы и методы: проанализированы результаты лечения 168 пациентов с нативной артериовенозной радиоцефальной фистулой. Прослежены результаты лечения в сроки до 1 года. Пациенты разделены на 2 группы: 1 группа — пациенты, у которых в течение 1 года гемодиализа не возникло тромбоза артериовенозной фистулы, 2 группа — пациенты, у которых в течение первого года произошла дисфункция постоянного сосудистого доступа вследствие тромбоза. Результаты: в рамках, сформулированной цели, определены факторы с наибольшей степенью влияния на риск возникновения тромбоза во временные промежутки до 6 месяцев и от 6 месяцев до 1 года. Однако не все они по своим характеристикам удовлетворяли условиям построения многомерной логистической регрессии и основанной на ней предсказательной модели. На основании выявленных факторов созданы прогностические модели, оценивающие риск возникновения тромбоза постоянного сосудистого доступа во временные промежутки до 6 месяцев и от 6 месяцев до 1 года. Заключение: Формирование предсказательной модели с учётом множества факторов способно дать ответ на риск формирования тромбоза и определить пути его уменьшения
Ключевые слова
Для цитирования:
Староверов Н.Н., Нощенко Н.С., Шубин Л.Б., Лончакова О.М. Прогнозирование риска тромбоза постоянного сосудистого доступа. Пациентоориентированная медицина и фармация. 2023;1(3):15-24. https://doi.org/10.37489/2949-1924-0020
For citation:
Staroverov I.N., Noshchenko N.S., Shubin L.B., Lonchakova O.M. Risk prediction for the thrombosis of permanent vascular access. Patient-Oriented Medicine and Pharmacy. 2023;1(3):15-24. (In Russ.) https://doi.org/10.37489/2949-1924-0020
Введение
В Российской Федерации ежегодный прирост числа больных, страдающих хронической почечной недостаточностью, соответствует общемировым тенденциям. В 2015 году в России заместительную почечную терапию получали свыше 44 тысяч больных с терминальной хронической почечной недостаточностью. Темп прироста больных в 2015 г. по отношению к предыдущему году составил 11,6%, что было выше среднего показателя за предыдущие 4 года (10,8%).
Показатель обеспеченности заместительной почечной терапией больных в пересчёте на 1 млн. населения, на 2015 год в среднем по России возрос до 301,2 больных на 1 млн.
Число больных, начавших заместительную почечную терапию в 2015 году, тоже увеличилось, по сравнению с предыдущими годами, и составило более 8,5 тысяч человек. Из них более 92% начали лечение программным гемодиализом [1]. Тенденция роста количества пациентов данной категории, увеличение продолжительности нахождения на гемодиализе повышает внимание к адекватному функционированию артериовенозной фистулы.
Остаётся до конца неразрешённым вопрос о причинах осложнений постоянного сосудистого доступа у пациентов с технически верным исполнением оперативного вмешательства. При формировании нативной артериовенозной фистулы продолжительность её работы составляет в среднем 3-5 лет и уменьшается в связи с развитием осложнений (тромбоз, стеноз, аневризма фистульной вены). Самым частым осложнением со стороны постоянного сосудистого доступа, от 60 до 90% случаев, является тромбоз артериовенозной фистулы [2]. В настоящее время разработан ряд правил использования постоянного сосудистого доступа, направленных на предотвращение таких осложнений, как тромбоз, кровотечение, инфекция постоянного сосудистого доступа, развитие аневризм фистульной вены. Проведено множество исследований по изучению факторов, влияющих на риск возникновения тромбоза. Таких как низкое сопротивление сосудистой стенки [3], продление антиагрегантной и антикоагулянтной терапии у пациентов на диализе [4][5], стенозов фистульной вены [6] и даже оценки влияния циркулирующих комплексов [7]. Остаётся множество не до конца изученных причин и механизмов возникновения осложнений постоянного сосудистого доступа, факторов, влияющих на частоту осложнений.
Цель: улучшить результаты хирургического лечения пациентов со сформированными первичными артериовенозными фистулами.
Задачи:
- Выявить предикторы тромбоза постоянного сосудистого доступа на дооперационном этапе.
- Оценить степень влияния выявленных предикторов на риск возникновения тромбоза постоянного сосудистого доступа.
- Создать прогностическую модель, позволяющую скорректировать риски тромбоза постоянного сосудистого доступа на дооперационном этапе.
Материалы и методы
Прослежены результаты лечения 168 пациентов с хронической болезнью почек в терминальной стадии. Из них 73 (43%) женщин и 95 (57%) мужчин. Средний возраст составил 56±14 лет. Прослежены результаты лечения пациентов до 1 года.
Каждому пациенту проводилось предоперационное обследование для определения локализации доступа в зависимости от состояния артериального и венозного русла в объёме ультразвукового исследования до и после проведения жгутовой пробы. Всем пациентам, включённым в исследование, формирование постоянного сосудистого доступа было произведено в нижней трети предплечья не доминантой верхней конечности. У всех пациентов в послеоперационном периоде отмечалось отчётливое систолодиастолическое дрожание анастомозированной вены.
В периоперационном периоде учитывались следующе параметры: диаметры артерии и вены, диаметр анастомоза, скорость кровотока в области анастомоза, стенозы фистульной вены экстравазального и интравазального типа, длительность антикоагулянтной терапии, применение антиагрегантов, коррекция и причины коррекции дозировки антикоагулянта, применение антибиотиков в послеоперационном периоде.
В дальнейшем, после «созревания» фистулы, всем пациентам проводилась заместительная почечная терапия. Всем пациентам проводился контроль лабораторных показателей согласно протоколу диализного центра клиники. В протокол исследования включены данные о показателях: степени снижения мочевины до и после диализа, гемоглобина, гематокрита, ферритина, использовании и дозировке эритропоэтина, железосодержащих препаратов и холекальциферола, уровнях натрия, калия, альбумина, паратиреоидного гормона, щелочной фосфатазы, кальция, фосфора, глюкозы, сухого веса пациента после сеанса гемодиализа, индекса массы тела, объёма ультрафильтрата, артериального давления до, во время и после сеанса гемодиализа.
Так же при дисфункции функционирующего постоянного сосудистого доступа пациентам проводился ультразвуковой контроль функционирования артериовенозной фистулы, на основе которого в исследование включены данные об аневризматическом расширении фистульной вены и наличии пристеночного тромбоза.
1. Определение факторов с наибольшей степенью влияния на риск возникновения тромбоза во временные промежутки до 6 месяцев и от 6 месяцев до 1 года
Первым этапом исследования выявлены особенности лабораторных показателей пациентов, находящихся на гемодиализе, которые могут быть прогностически значимыми факторами риска тромбоза постоянного сосудистого доступа. Об этом свидетельствуют следующие результаты, полученные в ходе исследования:
- выборка пациентов в начале исследования была однородна (p <0,05);
- в конце исследования группы различались по степени снижения мочевины, показателям калия, фосфора, глюкозы крови и сухого веса пациента (p <0,05). Данные показатели являются основными моделируемыми факторами риска тромбоза постоянного сосудистого доступа;
- при сравнении показателей пациентов в двух группах получены статистически достоверно значимые различия групп с тромбозом и без по показателям: мочевины до диализа, после диализа, эритропоэтина, препаратов железа, щелочной фосфатазы, фосфора, глюкозы крови, сухого веса, индекса массы тела (p <0,05);
- при анализе корреляций показателей с фактом возникновения тромбоза выявлена зависимость с дополнительным фактором — уровень альбумина (p <0,05);
- при контролируемом снижении показателей мочевины до диализа, после диализа, альбумина, щелочной фосфатазы, фосфора, глюкозы крови, сухого веса пациента достигается благоприятный прогноз длительности функционирования постоянного сосудистого доступа (p <0,05);
- при контролируемом повышении дозировки препаратов эритропоэтина и железа достигается благоприятный прогноз длительности функционирования постоянного сосудистого доступа (p <0,05).
Таким образом, систематический контроль данных показателей у пациентов, получающих заместительную почечную терапию посредством программного гемодиализа, может снизить процент тромбоза постоянного сосудистого доступа.
На втором этапе исследования учитывались факторы предоперационного, операционного и послеоперационного (до 1 года) состояния сосудистого русла, задействованного в постоянном сосудистом доступе и медикаментозного лечения. В рамках второго этапа определены критические промежутки функционирования постоянного сосудистого доступа. Ими явились промежуток функционирования фистулы до 6 месяцев и от 6 месяцев до 1 года, именно в эти периоды зафиксировано возрастающее количество тромбозов. Основными исход-зависимыми факторами риска, способствующими возникновению тромбоза постоянного сосудистого доступа вне зависимости критического периода, являются: атеросклероз; длительность антикоагулянтной терапии; коррекция антикоагулянтной терапии; антибиотикотерапия; диаметр фистульной вены; повторные операции; количество повторных операций; причина повторной операции.
Опираясь на выше сказанное, можно утверждать, что причины, приводящие к возникновению тромбоза постоянного сосудистого доступа до 6 месяцев и от 6 месяцев до 1 года, принципиально различны, это позволяет предположить, что реализация выделенных факторов риска, не является единственной причиной возникновения осложнений. Какие-то из процессов явно, либо не явно учитываемые при проведения данного исследования оказались вне зоны нашего влияния. Для более детального рассмотрения вероятности возникновения тромбоза постоянного сосудистого доступа в разные временные промежутки, видится целесообразным применение многомерного математического моделирования с просчётом и оценкой кумулятивного влияния предполагаемых предикторов на параметр отклик — факт возникновения осложнения (тромбоза).
2. Создание прогностической модели для расчёта риска тромбозов постоянного сосудистого доступа во временном промежутке до 6 месяцев
На основании выявленных факторов риска тромбоза постоянного сосудистого доступа решено построить многомерную математическую модель для уменьшения количества тромбозов постоянного сосудистого доступа, функционирующего в течение 6 месяцев [8]. Однако, при первичной попытке построения логистической регрессии устойчивой модели не было получено, ввиду выпадения единичных данных при формировании первичной базы данных, не зависящих от исследователей. В связи с чем произведена первичная редукция данных по строкам. В результате первичной редукции в построении логистической регрессии использованы данные 156 наблюдений.
Для построения модели использовался метод прямого пошагового исключения. В начале в модель включались исследуемые факторы. Оценивалось их совокупное влияние на исследуемое явление. Приемлемой считалась модель, отвечающая следующим параметрам:
- уровень значимости (p) самой модели ≤0,05;
- отношение шансов предикторов близкое к 1,0;
- коэффициент детерминации модели не ниже 0,63.
При выявлении фактора, не оказывающего достаточную степень влияния на исход, он исключался из модели. Процедура повторялась до выявления окончательной совокупности факторов, входящих в модель.
На основании множественного анализа в конечную модель логистической регрессии для снижения частоты тромбоза в промежутке функционирования постоянного сосудистого доступа до 6 месяцев вошли 8 параметров: длительность антикоагулянтной терапии, коррекция антикоагулянтной терапии, применение антибиотиков в послеоперационном периоде, уровень щелочной фосфатазы, калия, фосфора и альбумина в крови. Коэффициент детерминации модели составил: Cox & Snell — 0,66; Nagelkerke — 0,88.
Направленность влияния каждого из предикторов на изучаемое явление оценивалось по знаку коэффициента (плюс или минус): «+» отражал прямую направленность изменений между предиктором и прогнозируемым явлением; «-» обозначал обратную зависимость влияния фактора на исход прогнозируемого явления (т. е. уменьшение значения фактора увеличивало частоту прогнозируемого исхода). Результаты вычислений представлены в табл. 1.
Таблица 1. Коэффициенты влияния изучаемых факторов в период до 6 месяцев
Переменная | Коэффициент | Стандартная ошибка |
Длительность терапии | 1,05804 | 1,61222 |
Глюкоза | 1,35097 | 0,48133 |
Коррекция антикоагулянтной терапии | 2,06490 | 1,27422 |
Щелочная фосфатаза | 0,062998 | 0,012305 |
Калий | 1,52243 | 0,83416 |
Фосфор | -1,37676 | 1,34379 |
Антибиотикотерапия | 1,69713 | 0,96287 |
Альбумин | 0,034891 | 0,19468 |
При анализе полученных данных выявлено: показатель фосфора крови имеет обратную степень влияния на риск возникновения тромбоза, что объясняет повышение уровня фосфора в крови до 2,2±0,9 ммоль/л (в группе тромбоза) как увеличение риска возникновения тромбоза, а при нахождении данного показателя на уровне 1,7±0,4 ммоль/л (в группе без тромбоза) риск возникновения уменьшается. Оба этих параметра являются повышенными по отношению к норме 1,13±0,3 ммоль/л. Таким образом можно считать, что повышение уровня фосфора в крови выше 1,7±0,4 ммоль/л является прогностически неблагоприятным фактором в отношении тромбоза постоянного сосудистого доступа и требуется его коррекция в сторону уменьшения. Коэффициент влияния данного фактора равный -1,37676 определяет степень воздействия на факт тромбоза как высокое.
Показатели глюкозы имеют прямую зависимость с риском тромбоза. Таким образом повышение уровня глюкозы в группе с тромбозом до 5,78±2,6 ммоль/л, превышающую границы нормы, можно считать прогностически неблагоприятным фактором, увеличивающим риск тромбоза; а показатели, находящиеся в пределах нормы, в группе без тромбоза 3,6±0,8 ммоль/л, можно рассматривать как минимальный риск тромбоза. Коэффициент влияния данного фактора равный 1,35097 определяет степень воздействия на факт тромбоза как высокое.
Показатели щелочной фосфатазы имеют прямую зависимость с риском тромбоза. В группе без тромбоза они составляли 94±14,1 МЕ/л и находились в пределах нормы, а в группе с тромбозом 172±42,8 МЕ/л — превышали норму до 2 раз. Учитывая это, можно предполагать, что превышение верхней границы нормы показателей щелочной фосфатазы является прогностически неблагоприятным фактором возникновения тромбоза постоянного сосудистого доступа. Коэффициент влияния данного фактора равный 0,062998 определяет степень воздействия на факт тромбоза как низкое.
Показатели калия так же имеют прямую зависимость с риском тромбоза. В группе без тромбоза они составляли 5,5±0,6 ммоль/л, что является верхней границей нормы; а в группе с тромбозом — 5,92±0,8 ммоль/л. Исходя из этих показателей так же можно предполагать, что повышения уровня калия в крови, а особенно превышение верхней границы его нормы является фактором, увеличивающим риск наступления тромбоза артериовенозной фистулы. Коэффициент влияния данного фактора равный 0,034891 определяет степень воздействия на факт тромбоза как низкое.
Показатель альбумина крови имеет прямую зависимость с риском тромбоза. В группе без тромбоза он составлял 38±3,6 г/л, с тромбозом — 40±2,7 г/л. Оба эти параметра находятся в переделах нормальных значений. Коэффициент влияния данного фактора равный 1,35097 определяет степень воздействия на факт тромбоза как высокое.
Увеличение длительности антикоагулянтной терапии имело прямую зависимость с риском тромбоза. Применение антикоагулянтов в профилактической дозе после оперативного вмешательства более 10 дней не только не приводило к снижению риска тромбоза, а наоборот его повышало. Коэффициент влияния данного фактора равный 1,05804 определяет степень воздействия на факт тромбоза как высокое.
Коррекция антикоагулянтной терапии в послеоперационном периоде также имела прямую зависимость с фактом тромбоза. Следовательно, изменение дозировки антикоагулянта отличной от профилактической повышает риск тромбоза. Коэффициент влияния данного фактора равный 2,06490 определяет степень воздействия на факт тромбоза как высокое.
Применение профилактической антибиотикотерапии в послеоперационном периоде находится в прямой зависимости от риска тромбоза и, следовательно, отсутствие антибиотикопрофилактики повышает риск возникновения тромбоза. Коэффициент влияния данного фактора равный 1,69713 определяет степень воздействия на факт тромбоза как высокое.
Что бы понять на сколько часто исследуемые параметры в своей совокупности оказывают влияние на факт возникновения тромбоза, были рассчитаны отношения шансов реализации используемых в модели факторов. Сводная таблица и сводная Форест-диаграмма вычисленного отношения шансов реализации факторов в прогностической модели для критического промежутка 6 месяцев представлены ниже (см. табл. 2 и рис. 1).
Таблица 2. Отношение шансов реализации факторов
в прогностической модели для критического периода 6 месяцев
Фактор | Отношение шансов | ДИ -95% | ДИ +95% |
Длительность терапии | 2,8807 | 0,1222 | 67,8976 |
Глюкоза | 3,8612 | 1,5032 | 9,9182 |
Щелочная фосфатаза | 1,0650 | 1,0396 | 1,0910 |
Коррекция антикоагулянтной терапии | 7,8845 | 0,6488 | 95,8102 |
Антибиотикотерапия | 5,4583 | 0,8269 | 36,0299 |
Калий | 4,5834 | 0,8936 | 23,5088 |
Фосфор | 0,2524 | 0,0181 | 3,5151 |
Альбумин | 1,0355 | 0,7070 | 1,5166 |
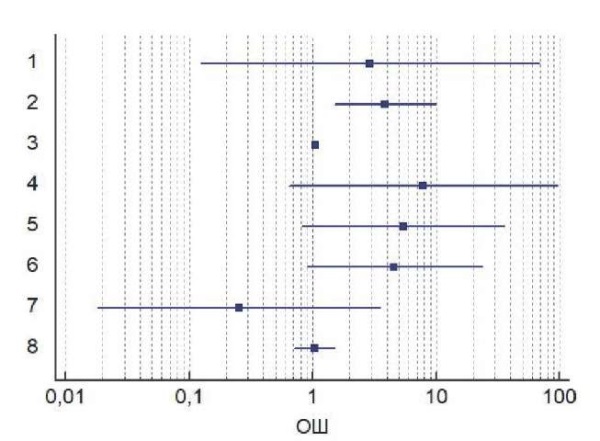
Рис. 1. Отношение шансов реализации факторов
в прогностической модели для критического периода 6 месяцев
Примечания: 1 — длительность терапии; 2 — глюкоза;
3 — щелочная фосфатаза; 4 — коррекция антикоагулянтной терапии;
5 — антибиотикотерапия; 6 — калий; 7 — фосфор; 8 — альбумин.
Результатом уравнения множественной логистической регрессии являлось числовое значение ассоциированного критерия. Числовое значение ассоциированного критерия анализировалось в ROC-анализе для определения прогноза по оцениваемой многомерной модели.
Модель прогноза изучаемого явления (тромбоза постоянного сосудистого доступа в течение 6 месяцев) по значениям исследуемых параметров формировали с помощью ROC-анализа. Он отражал взаимоотношение чувствительности и специфичности при различных значениях исследуемых факторов в виде характеристической кривой [9][10].
Чувствительность определяли, как долю истинно положительных случаев определения тромбоза в общем объёме положительных результатов. Специфичность определяли, как долю истинно отрицательных результатов (отсутствие тромбоза) в общем объёме отрицательных показателей.
Значимость прогноза определяли по площади под характеристической кривой AUC (Area Under Curve). Эту площадь оценивали в приделах от 0,5 («бесполезный» тест) до 1,0 («идеальный» тест). Качество полученного прогноза характеризовали по экспертной шкале значений AUC [11] представленной в табл. 3.
Таблица 3. Интерпретация значений AUC
Интервал AUC | Качество модели |
1,0 – 0,9 | отличное качество |
0,9 – 0,8 | высокое качество |
0,8 – 0,7 | хорошее качество |
0,7 – 0,6 | среднее качество |
0,6 – 0,5 | удовлетворительное качество |
Полученные результаты характеризовались высокой чувствительностью и специфичностью. Качество модели расценивалось как «отличное». Результат оценки представлен на рис. 2.
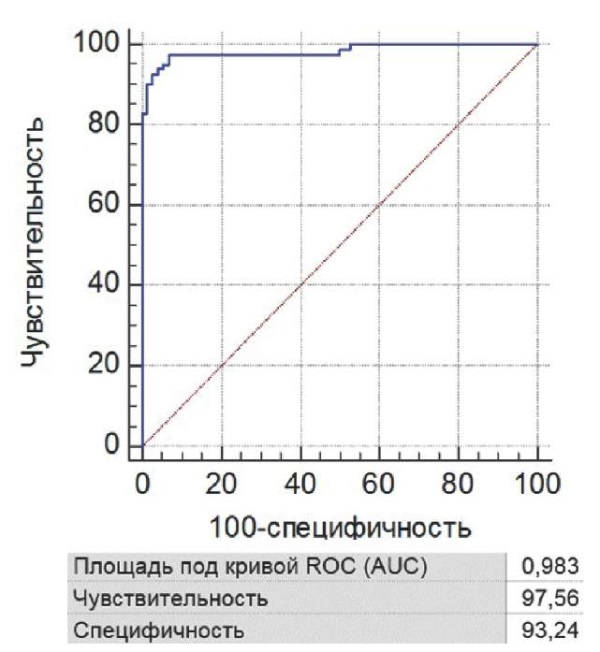
Рис. 2. ROC-анализ прогностической модели для расчёта
риска тромбозов постоянного сосудистого доступа
во временном промежутке до 6 месяцев
Полученный результат свидетельствует о высокой эффективности разработанной модели для прогнозирования риска тромбоза постоянного сосудистого доступа в промежутке функционирования до 6 месяцев, что позволяет с большой долей уверенности спрогнозировать наличие или отсутствие тромбоза в данный критический период.
3. Создание прогностической модели для расчёта риска тромбозов постоянного сосудистого доступа во временном промежутке от 6 месяцев до 1 года
С учётом малого периода прогноза при формировании предыдущей модели, нарастания количества тромбозов постоянного сосудистого доступа во временном промежутке свыше 6 месяцев, при низком риске тромбоза рассчитанном на период до 6 месяцев, принято решение построить модель на основании исходных данных для прогнозирования риска тромбоза во временном промежутке от 6 месяцев до 1 года.
Однако при первичной попытке построения логистической регрессии устойчивой модели не было получено, ввиду низкой специфичности и чувствительности полученной модели. В связи с чем произведена вторичная редукция данных, обусловленных ошибками классификации. В результате вторичной редукции в построении логистической регрессии использованы данные 135 наблюдений.
Для построения модели так же, как и в предыдущем случае использовался метод прямого пошагового исключения. С теми же требованиями к конечной модели. Процедура повторялась до выявления окончательной совокупности факторов, входящих в модель.
На основании множественного анализа в конечную модель логистической регрессии для снижения частоты тромбоза в промежутке функционирования постоянного сосудистого доступа от 6 месяцев до 1 года вошли 8 параметров: диаметр фистульной вены при формировании анастомоза, применение антибиотикотерапии, мочевина крови до и после сеанса диализа, уровень фосфора крови, наличие в анамнезе повторных операций на фистульной вене и причины этих операций, а также применение эритропоэтина. Коэффициент детерминации модели составил: Cox & Snell — 0,51; Nagelkerke — 0,69.
Направленность влияния каждого из предикторов на изучаемое явление оценивалось по знаку коэффициента, так же, как и в предыдущей модели. Результаты вычислений представлены в табл. 4.
Таблица 4. Коэффициенты влияния изучаемых факторов
в период от 6 месяцев до 1 года
Переменная | Коэффициент | Стандартная ошибка |
Фосфор | 2,31615 | 0,71472 |
Антибиотикотерапия | 4,18636 | 1,03348 |
Диаметр вены | -0,27359 | 0,60262 |
Мочевина до диализа | 0,098263 | 0,092679 |
Мочевина после диализа | 0,053415 | 0,20179 |
Повторные операции | 4,63464 | 1,32669 |
Причина повторных операций | -8,06961 | 1,88875 |
Применение эритропоэтина | -0,00023359 | 0,00012666 |
При анализе полученных данных выявлено, что диаметр фистульной вены находится в обратной зависимости от риска тромбоза, следовательно, чем больше диаметр фистульной вены при формировании анастомоза, тем ниже риск тромбоза; а коэффициент влияния данного параметра равный -0,27359 определяет степень воздействия на факт тромбоза как среднюю (низкую).
Применение профилактической антибиотикотерапии в послеоперационном периоде находится в прямой зависимости от риска тромбоза и, следовательно, отсутствие антибиотикопрофилактики повышает риск возникновения тромбоза; а коэффициент влияния данного параметра равный 4,18636 определяет степень воздействия на факт тромбоза как высокую.
Уровень мочевины крови до диализа имеет прямую зависимость с риском тромбоза. В группе без тромбоза этот показатель был равен 22±6,1 ммоль/л, а в группе с тромбозом — 27±6,7 ммоль/л. В обеих группах данный показатель значительно превышал возрастные нормы. Хотя различие уровня мочевины составляло всего 5 ммоль/л в сравниваемых группах, данный интервал коррелируется с допустимым диапазоном значений при нормальном значении мочевины крови. Следовательно, можно считать данное различие значимым. Однако коэффициент влияния данного параметра равный 0,098263 определяет степень воздействия на факт тромбоза как низкую.
Уровень мочевины после сеанса диализа так же имеет прямую зависимость с фактом тромбоза. В группе без тромбоза уровень мочевины был 7,8±2,4 ммоль/л, а в группе с тромбозом — 9,2±2,9 ммоль/л. В первой группе уровень мочевины характеризовался как норма, а вот во второй группе превышал верхнее пороговое значение. Следовательно, достижение нормальных значений уровня мочевины после диализа является благоприятным прогностическим фактором тромбоза фистулы. Хотя коэффициент влияния данного параметра равный 0,053415 и определяет степень воздействия на факт тромбоза как низкую.
Уровень фосфора крови в отличие от модели для периода до 6 месяцев имеет прямую зависимость с фактом тромбоза. В группе без тромбоза он составлял 1,69±0,3 ммоль/л, а в группе с тромбозом — 2,21±0,9 ммоль/л. В обоих случаях уровень фосфора был выше нормы, но в группе с тромбозом превышал верхнюю границу в 2-3 раза. Из чего можно сделать заключение, что на фоне диализа высокие показатели фосфора крови являются неблагоприятными и способствуют увеличению риска тромбоза. Коэффициент влияния данного параметра равный 2,31615 определяет степень воздействия на факт тромбоза как высокую.
Наличие в анамнезе повторных операций на фистульной вене также имело прямую зависимость с фактом тромбоза и повышало риск тромбоза.
Однако операции, не сопровождавшиеся первоначальным тромбозом, например, из-за высокого сброса по притокам или аневризматического расширения, снижали уровень риска прогнозируемого тромбоза. Коэффициенты влияния этих параметров равные 4,63464 и -8,06961, соответственно, определяют степень их воздействия на факт тромбоза как высокую.
Доза эритропоэтина имела обратную зависимость с фактом тромбоза. В группе без тромбоза средний показатель недельной дозировки эритропоэтина для пациентов с анемией составил 5488±2579 МЕ/кг, а в группе с тромбозом — 4554±2164 МЕ/кг. Таким образом у пациентов, получающих более высокую дозировку эритропоэтина, при наличии показаний, риск возникновения тромбоза снижался. Коэффициент влияния этого параметр равный -0,00023359 определяет степень воздействия на факт тромбоза как очень низкую. По-видимому, это обусловлено малым количеством наблюдений и узким спектром показаний к назначению данного препарата.
Что бы понять на сколько часто исследуемые параметры в своей совокупности оказывают влияние на факт возникновения тромбоза, так же были рассчитаны отношения шансов реализации используемых в модели факторов. Сводная таблица и сводная Форест-диаграмма вычисленного отношения шансов реализации факторов в прогностической модели для критического промежутка от 6 месяцев до 1 года представлены ниже (см. табл. 5 и рис. 3).
Таблица 5. Отношение шансов реализации факторов в прогностической модели
для критического периода от 6 месяцев до 1 года
Фактор | Отношение шансов | ДИ -95% | ДИ +95% |
Фосфор | 10,1365 | 2,4975 | 41,1407 |
Антибиотикотерапия | 65,7829 | 8,6775 | 498,6904 |
Диаметр вены | 0,7606 | 0,2335 | 2,4782 |
Мочевина до диализа | 1,1033 | 0,9200 | 1,3230 |
Мочевина после диализа | 1,0549 | 0,7103 | 1,5666 |
Повторные операции | 102,9913 | 7,6472 | 1387,0680 |
Причина повторных операций | 0,0003 | 0,0000 | 0,0127 |
Применение эритропоэтина | 0,9998 | 0,9995 | 1,0000 |
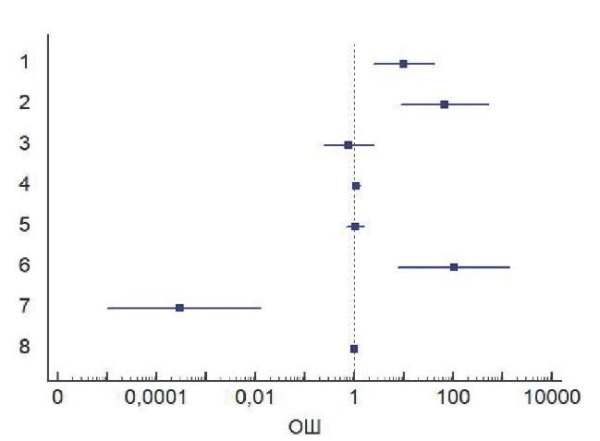
Рис. 3. Отношение шансов реализации факторов
в прогностической модели для критического периода от 6 месяцев до 1 года
Примечания: 1 — фосфор; 2 — антибиотикотерапия;
3 — диаметр вены; 4 — мочевина до диализа;
5 — мочевина после диализа; 6 — повторные операции;
7 — причина повторных операций; 8 — применение эритропоэтина.
Результатом уравнения множественной логистической регрессии являлось числовое значение ассоциированного критерия. Числовое значение ассоциированного критерия анализировалось в ROC-анализе для определения прогноза по оцениваемой многомерной модели.
Модель прогноза изучаемого явления (тромбоза постоянного сосудистого доступа в промежутке времени от 6 месяцев до 1 года) по значениям исследуемых параметров формировали с помощью ROC-анализа. По тем же критериям, что использовались для модели критического промежутка времени до 6 месяцев.
На основании данных, полученных в результате построения логистической регрессии, был проведен ROC-анализ. Полученные результаты характеризовались высокой чувствительностью и специфичностью. Качество модели расценивалось как «высокое». Результат оценки представлен на рис. 4.
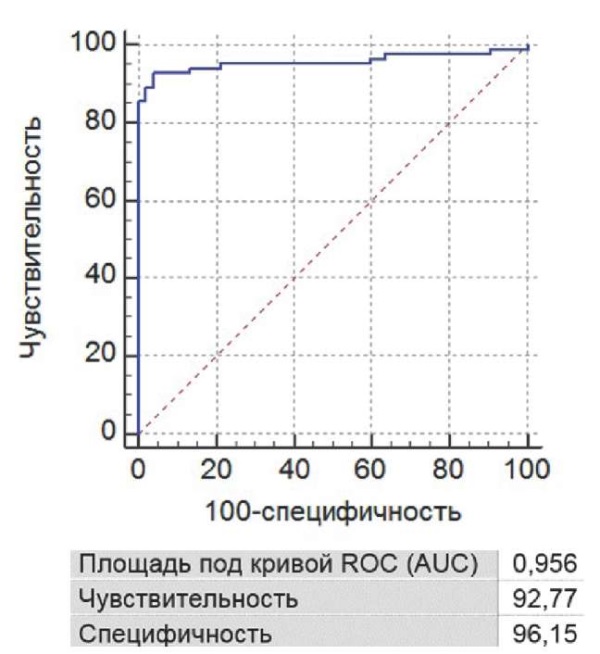
Рис. 4. ROC-анализ прогностической модели для расчёта
риска тромбозов постоянного сосудистого доступа
во временном промежутке от 6 месяцев до 1 года
Полученный результат свидетельствует о высокой эффективности разработанной модели для прогнозирования риска тромбоза постоянного сосудистого доступа в промежутке функционирования от 6 месяцев до 1 года. Однако с учётом низкого коэффициента детерминации модели прогнозирование вероятности тромбоза на столь долгий срок при получении лишь периоперационных данных без детальной оценки состояния сосудистого русла в динамике требует более углубленного изучения.
Обсуждения и выводы
В рамках сформулированной цели, определены факторы с наибольшей степенью влияния на риск возникновения тромбоза во временные промежутки до 6 месяцев и от 6 месяцев до 1 года. Однако не все они по своим характеристикам удовлетворяли условиям построения многомерной логистической регрессии и основанной на ней предсказательной модели.
Учитывая вышеизложенное, можно с уверенностью сказать, что формирование предсказательной модели с учётом множества, по отдельности малозначимых предикторов, в своей совокупности факторов способно дать ответ на риск формирования искомого результата.
В условиях данного исследования можно с определённо высокой долей вероятности утверждать, что полученная нами прогностическая модель для расчёта риска тромбоза постоянного сосудистого доступа во временной промежуток до 6 месяцев показала себя устойчивой и может применятся в расчётах в реальной клинической практике. С другой стороны, модель для расчёта риска тромбозов во временной промежуток времени от 6 месяцев до 1 года обладает меньшей степенью достоверности и при расчётах может выдавать достаточно высокий процент неверных заключений. Однако, попытка прогнозирования тромбоза постоянного сосудистого доступа на такой долгий срок, зависящая от большого количества переменных, достаточно успешна.
Для построения более устойчивой модели долгосрочного прогнозирования тромбоза требуется накопление информации о функционировании постоянного сосудистого доступа на всём протяжении наблюдения вне зависимости от наступления каких-либо неблагоприятных условий. Этот факт даёт множество вариантов для проведения более углублённого изучения данной проблемы.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Участие авторов
Все авторы внесли существенный вклад в подготовку работы, прочли и одобрили финальную версию статьи перед публикацией. Староверов И.Н. — концепция и дизайн исследования, сбор и обработка материала, ответственность за целостность всех частей статьи, написание текста; Нощенко Н.С., Шубин Л.Б. — статистическая обработка данных, редактирование; Лончакова О.М. — сбор и обработка материала, редактирование.
Финансирование
Работа выполнялась без спонсорской поддержки.
ADDITIONAL INFORMATION
Conflict of interests
The authors declare no conflict of interest.
Authors’ participation
All authors made a significant contribution to the preparation of the work, read, and approved the final version of the article before publication. Staroverov IN — study concept and design, collection and processing of data, responsibility for the integrity of all parts of the article, writing the text; Noshchenko NS, Shubin LB — statistical data processing, editing; Lonchakova OM — collection and processing of data, editing.
Acknowledgments
The work was carried out without sponsorship.
Список литературы
1. Томилина Н.А., Андрусев А.М., Перегудова Н.Г., Шинкарев М.Б. Заместительная терапия терминальной хронической почечной недостаточности в Российской Федерации в 2010-2015 гг. Отчет по данным Общероссийского Регистра заместительной почечной терапии Российского диализного общества, Часть первая. Нефрология и диализ. 2017. 19(4):1-95. doi: 10.28996/1680-4422-2017-4suppl-1-95 [Tomilina N.A., Andrusev A.M., Peregudova N.G., Shinkarev M.B. Renal replacement therapy for End Stage Renal Disease in Russian Federation, 2010-2015. Russian National Renal Replacement Therapy Registry Report of Russian Public Organization of Nephrologists "Russian Dialysis Society", Part 1. Nephrology and dialysis. 2017. 19(4):1-95. doi: 10.28996/1680-4422-2017-4suppl-1-95]
2. Стецюк Е.А. Основы гемодиализа. ГЭОТАР–МЕД. – М. : Изд–во ГЭОТАР–МЕД, 2001. – 392с. [Stecyuk E.A. Osnovy gemodializa. GEHOTAR–MED. – M. : Izd–vo GEHOTAR–MED, 2001. – 392s.]
3. Smith GE, Barnes R, Fagan M, Chetter IC. The Impact of Vein Mechanical Compliance on Arteriovenous Fistula Outcomes. Ann Vasc Surg. 2016 Apr;32:9-14. doi: 10.1016/j.avsg.2015.11.002. Epub 2016 Jan 25. PMID: 26820359.
4. Yeh CH, Huang TS, Wang YC, Huang PF, Huang TY, Chen TP, Yin SY, Yu YW. Effects of Antiplatelet Medication on Arteriovenous Fistula Patency After Surgical Thrombectomy. Curr Vasc Pharmacol. 2016;14(4):353-9. doi: 10.2174/1570161114666160229115844. PMID: 26924326.
5. Tanner NC, Da Silva A. Medical adjuvant treatment to increase patency of arteriovenous fistulae and grafts. Cochrane Database of Systematic Reviews. 2015, Issue 7. Art. No.: CD002786. DOI: 10.1002/14651858.CD002786.pub3. Accessed 22 August 2023.
6. King DH, Paulson WD, Al-Qaisi M, Taylor MG, Panayiotopoulos Y, Abeygunarsekara S, Chan A, Ali G, Chemla ES. Volume blood flow, static pressure ratio and venous conductance in native arterio-venous fistulae: three surveillance methods compared. J Vasc Access. 2015 May-Jun;16(3):211-7. doi: 10.5301/jva.5000324. Epub 2015 Jan 30. PMID: 25656259.
7. Morton SK, Rodríguez AJ, Morris DR, Bhandari AP, Moxon JV, Golledge J. A Systematic Review and Meta-Analysis of Circulating Biomarkers Associated with Failure of Arteriovenous Fistulae for Haemodialysis. PLoS One. 2016 Jul 26;11(7):e0159963. doi: 10.1371/journal.pone.0159963. PMID: 27458819; PMCID: PMC4961283.
8. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA – М.: Медиасфера, – 2002, – 312 с. [Rebrova O.YU. Statisticheskij analiz meditsinskikh dannykh. Primenenie paketa prikladnykh programm STATISTICA – Moscow: Mediasfera, – 2002, – 312 s. (In Russ).]
9. Robert H. Fletcher, Suzanne W. Fletcher, Edward Harris Wagner. Clinical Epidemiology: The Essentials. Williams & Wilkins, 1996. – 352s
10. Плещёв И. Е., Николенко В. Н., Ачкасов Е. Е., Шкребко А. Н. Алгоритм применения индивидуально — группового протокола при комплексной реабилитации пациентов с саркопенией. Вестник «Биомедицина и Социология». 2022;24(5):44-53. doi:10.26787/nydha-2618-8783-2022-7-2-44-53.
11. Румянцев П.О., Саенко В.А., Румянцева У.В., Чекин С.Ю. Статистические методы анализа в клинической практике. ГУ-Медицинский радиологический научный центр РАМН, г. Обнинск. 2009. – 44 с. [Rumyancev P.O., Saenko V.A., Rumyanceva U.V., Chekin S.Yu. Statisticheskie metody analiza v klinicheskoy praktike. GU-Medicinskiy radiologicheskiy nauchnyy centr RAMN, g. Obninsk. 2009. – 44 s.]
Об авторах
Н. Н. СтароверовРоссия
Староверов Илья Николаевич — д. м. н., зав. отделением сосудистой хирургии, зав. кафедрой хирургии
РИНЦ Author ID: 717973
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Н. С. Нощенко
Россия
Нощенко Никита Сергеевич — к. м. н., ассистент кафедры хирургии
РИНЦ Author ID: 1015260
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Л. Б. Шубин
Россия
Шубин Леонид Борисович — к. м. н., доцент, кафедра патологической анатомии
РИНЦ Author ID: 484053
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
О. М. Лончакова
Россия
Лончакова Оксана Михайловна — к. м. н., доцент кафедры хирургии
РИНЦ Author ID: 915633
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Староверов Н.Н., Нощенко Н.С., Шубин Л.Б., Лончакова О.М. Прогнозирование риска тромбоза постоянного сосудистого доступа. Пациентоориентированная медицина и фармация. 2023;1(3):15-24. https://doi.org/10.37489/2949-1924-0020
For citation:
Staroverov I.N., Noshchenko N.S., Shubin L.B., Lonchakova O.M. Risk prediction for the thrombosis of permanent vascular access. Patient-Oriented Medicine and Pharmacy. 2023;1(3):15-24. (In Russ.) https://doi.org/10.37489/2949-1924-0020
JATS XML


































.png)
