Перейти к:
Современное экстемпоральное фармацевтическое производство: проблемы и перспективы
https://doi.org/10.37489/2949-1924-0049
EDN: LCXGIU
Аннотация
Актуальность. Экстемпоральное изготовление лекарственных препаратов — одна из важных составляющих в современной пациентоориентированной медицине. В статье приведён анализ нормативно-правовых документов, регулирующих изготовление лекарственных препаратов в условиях аптеки, обозначены, проблемы и слабые стороны нормирования производства, а также предложены конструктивные пути решения представленных проблем.
Методология. При выполнении исследования использовались методы контент-анализа, сравнительного и логического анализа, наблюдения.
Результаты. В статье был приведён критический анализ нормативно-правовой базы, регламентирующей экстемпоральное производство лекарственных препаратов. Выявлены слабые стороны в регулировании аптечного производства лекарственных форм. В частности, представлены проблемы, связанные с фармацевтической экспертизой рецепта: с проверкой доз активных фармацевтических субстанций и оценкой совместимости ингредиентов прописи; вопросы связанные со сроками годности экстемпорально изготовленных лекарственных препаратов; проблемы с нормированием условий изготовления лекарств в аптеке. Отражены трудности с оснащением аптек средствами малой механизации, аспекты обеспеченности современными активными фармацевтическими ингредиентами и вспомогательными веществами, отмечен потенциал врачей в вопросах выписывания экстемпоральной рецептуры.
Заключение. Предложенные пути решения обозначенных проблем позволят вывести экстемпоральное производство на новый, более совершенный уровень и расширить возможности персонифицированной медицины.
Ключевые слова
Для цитирования:
Чикина И.В., Онегин С.В., Парфенов А.А., Трубников А.А. Современное экстемпоральное фармацевтическое производство: проблемы и перспективы. Пациентоориентированная медицина и фармация. 2024;2(2):43-50. https://doi.org/10.37489/2949-1924-0049. EDN: LCXGIU
For citation:
Chikina I.V., Onegin S.V., Parfenov A.A., Trubnikov A.A. Modern extemporaneous pharmaceutical manufacturing: problems and prospects. Patient-Oriented Medicine and Pharmacy. 2024;2(2):43-50. (In Russ.) https://doi.org/10.37489/2949-1924-0049. EDN: LCXGIU
Актуальность / Relevance
Быстрорастущим мировым трендом в современной медицине является персонифицированный подход в лечении пациентов с различными заболеваниями, который учитывает индивидуальные особенности каждого человека и позволяет подобрать наиболее эффективную и безопасную терапию. Глубокое, подробное и полное изучение состояния здоровья пациента, персонально подобранные схемы терапии, своевременная профилактика заболеваний являются обязательными атрибутами такого подхода. Персонифицированная медицина основана на утверждении, что каждый человек обладает уникальными характеристиками на молекулярном, физиологическом, экологическом и поведенческом уровнях, и в случае развития болезни её лечение следует проводить с учётом этих уникальных характеристик [1][2]. Индивидуальный подход к лечению пациентов обладает существенными преимуществами перед традиционным популяционным методом. Неоспорима ценность данного подхода в педиатрической и геронтологической практиках. Однако данная концепция сложна для реализации в существующей системе здравоохранения Российской Федерации [3–5].
Экстемпоральное производство индивидуальных лекарственных препаратов является неотъемлемой частью персонифицированного подхода. Рецептурно-производственные отделы (РПО) аптек позволяют удовлетворить потребность пациентов в лекарственных препаратах, не имеющих аналогов в промышленном производстве, обеспечивают индивидуальное дозирование лекарственных веществ с учётом особенности пациента.
Вместе с тем, нормативно-правовая база, регламентирующая данную сферу деятельности, имеет достаточное количество спорных моментов, неясностей и противоречий. Для гармонизации регуляторных требований необходимо обозначение слабых сторон и возможностей для улучшения процесса изготовления, что требует организационной и методической поддержки со стороны Минздрава РФ, а также активного участия фармацевтического сообщества в дискуссиях и разработке необходимой документации, актуализации существующих норм и правил [6–8].
Стимулирование развития аптечного изготовления позволит улучшить доступность лекарственной помощи населению с учётом индивидуальных дозировок и лекарственных форм в различных терапевтических направлениях [9].
Кроме того, требуют решения вопросы расширения аптечного ассортимента фармацевтических субстанций и вспомогательных веществ, новых упаковочных материалов, использование современных разработок в этом вопросе [10].
Несомненно, острой является проблема рентабельности аптечного изготовления, требующая государственной поддержки и процессов финансовой оптимизации деятельности аптек [11].
Цель / Objective
Целью настоящего исследования является выявление и обозначение проблем в современном экстемпоральном производстве лекарственных препаратов, как неотъемлемой части персонифицированной медицины, а также предложение путей решения представленных проблем и возможностей для улучшения процесса аптечного изготовления лекарств.
Задачи / Tasks
Провести анализ нормативно-правовой базы регулирования экстемпорального производства лекарственных препаратов; изложить перечень конструктивных предложений для оптимизации регулирования экстемпорального производства.
Методология / Methodology
В работе использовались методы контент-анализа, сравнительного и логического анализа, наблюдения. Объектами послужили данные сайтов — электронных фондов нормативно-технической и нормативно-правовой информации, нормативно-правовые акты, регламентирующие экстемпоральное изготовление лекарственных препаратов [12–18].
Результаты / Results
Существующий алгоритм фармацевтической экспертизы рецепта включает в себя несколько обязательных этапов, при этом корректное выполнение отдельных из них на сегодняшний день не представляется возможным.
Проанализировав нормативно-правовую базу, регламентирующую порядок назначения лекарственных препаратов, формы рецептурных бланков на лекарственные препараты, порядок оформления указанных бланков, их учёта и хранения форм бланков рецептов, содержащих назначение наркотических средств или психотропных веществ, порядок их изготовления, распределения, регистрации, учёта и хранения, а также правила оформления бланков рецептов, в том числе в форме электронных документов [14] и правила отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на осуществление фармацевтической деятельности, медицинскими организациями, имеющими лицензию на осуществление фармацевтической деятельности, и их обособленными подразделениями (амбулаториями, фельдшерскими и фельдшерско-акушерскими пунктами, центрами (отделениями) общей врачебной (семейной) практики), расположенными в сельских поселениях, в которых отсутствуют аптечные организации, а также правила отпуска наркотических средств и психотропных веществ, зарегистрированных в качестве лекарственных препаратов для медицинского применения, лекарственных препаратов для медицинского применения, содержащих наркотические средства и психотропные вещества, в том числе порядок отпуска аптечными организациями иммунобиологических лекарственных препаратов [15], нами отмечено, что в приказах отсутствуют положения, связанные с проверкой доз и совместимостью прописанных в рецепте ингредиентов. При этом, общая фармакопейная статья ОФС. 1.8.0001 «Лекарственные препараты аптечного изготовления» действующей Государственной фармакопеи требует проверки совместимости веществ и соответствия прописанных доз возрасту пациента в магистральных прописях [16]. По нашему мнению, проверка доз активных фармацевтических ингредиентов в рецепте — важный этап фармацевтической экспертизы, связанный с дополнительным контролем непреднамеренно завышенного количества выписанных лекарственных веществ.
При проверке доз фармацевтический работник сталкивается с проблемой отсутствия действующих нормативных документов, в которых приведены установленные высшие разовые и высшие суточные дозы (ВРД и ВСД) на субстанции, используемые в экстемпоральном изготовлении. На данном этапе при проверке доз используются устаревшие сведения из Государственной фармакопеи СССР X издания или терапевтические дозы из инструкций на готовые лекарственные препараты.
При проведении фармацевтической экспертизы рецепта, на наш взгляд, этап проверки совместимости ингредиентов прописи также затруднён, что связано с отсутствием понятного алгоритма и современных данных по физическому, химическому и фармакологическому взаимодействию между ингредиентами прописи.
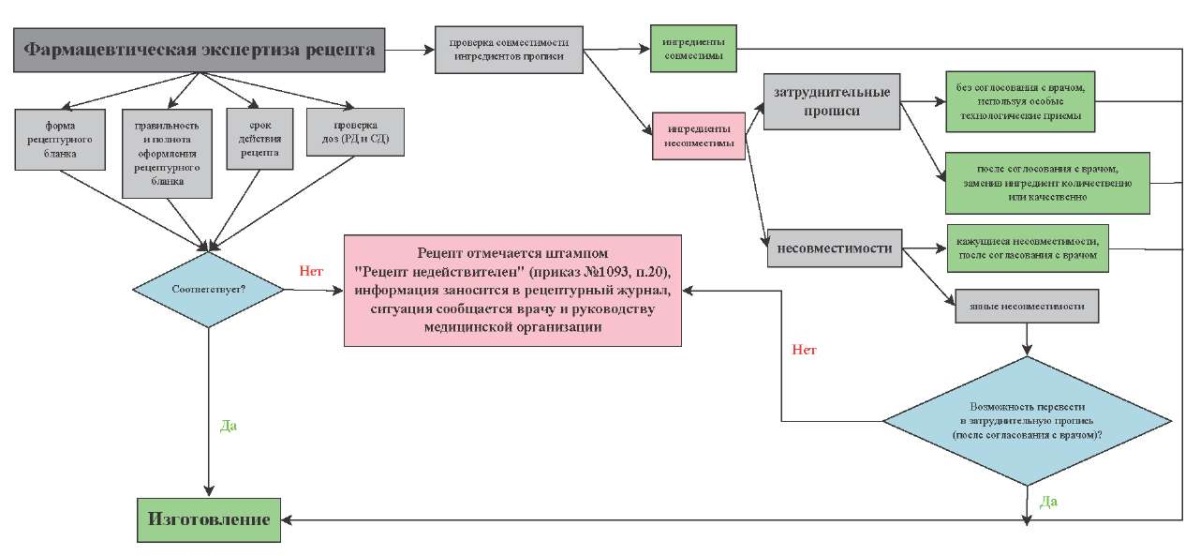
Диаграмма. Алгоритм фармацевтической экспертизы
рецепта на экстемпоральную лекарственную форму
Diagram. Algorithm for pharmaceutical examination
of a prescription for an extemporaneous dosage form
В связи с этим, предлагаем разработанный сотрудниками кафедры фармакогнозии и фармацевтической технологии ЯГМУ алгоритм фармацевтической экспертизы рецепта на экстемпоральную лекарственную форму (см. диаграмму). Кроме того, считаем необходимым разработку и внедрение нормативного документа, регламентирующего дозы (ВРД и ВСД) для активных фармацевтических субстанций, в том числе с учётом возрастных особенностей пациентов. При создании данного документа необходимо совместное участие медицинских и фармацевтических специалистов, использование действующих клинических рекомендаций и современных данных о терапии заболеваний. Также требуется актуализировать и обобщить информацию о совместимости используемых фармацевтических субстанций.
Важно отметить, что одним из острых и широко дискутируемых вопросов в фармацевтическом сообществе является проблема сроков годности экстемпорально изготовленных лекарственных средств. С одной стороны, установленные действующими нормативными документами [13][16] временные интервалы хранения достаточны для экстемпоральных лекарственных препаратов, изготовленных по индивидуальным рецептам или требованиям. С другой стороны, эти же сроки ограничивают возможности аптеки при реализации внутриаптечной заготовки лекарственных препаратов, изготовленных заранее по часто встречающимся прописям. Также возникает проблема со сроками годности для экстемпоральных лекарственных препаратов в случаях транспортировки в отдалённые от аптечного учреждения регионы страны. В связи с этим, считаем необходимым предоставить аптеке возможность самостоятельно изменять или устанавливать сроки годности, подтверждая стабильность лекарственного препарата экспериментальными данными. Подобные исследования необходимо проводить, исключительно в аккредитованных специализированных лабораториях, имеющих утверждённые регламенты по изучению стабильности лекарственных средств.
Условия экстемпорального изготовления в настоящее время регламентируются отдельными требованиями в разных нормативных документах [16][18]. По нашему мнению, уровень детализации требований недостаточна. В следствии этого аптека вынуждена самостоятельно разрабатывать стандартные операционные процедуры (СОП) по соблюдению правил санитарного режима. Такая степень свободы в соблюдении условий изготовления может приводить к ненадлежащему обеспечению качества изготовленных лекарственных форм. В связи с этим, предлагаем унифицировать подходы к реализации условий изготовления экстемпоральных лекарственных форм созданием единого стандарта.
Экстемпоральное производство, даже в современных условиях, подразумевает использование большого количества ручного труда фармацевта или провизора. При этом, внедрение средств малой механизации и оборудования для мелкосерийного производства позволит существенно увеличить производительность труда, повысить технологичность процесса и минимизировать влияние человеческого фактора, а также отчасти снизить себестоимость экстемпорального лекарственного препарата. Тем не менее, современная аптека не может в полной мере использовать средства малой механизации, так как рынок данного оборудования характеризуется скудным ассортиментом, отсутствием адаптации к нуждам рецептурно-производственных аптек и высокой стоимостью.
Одним из главных факторов, сдерживающих развитие экстемпорального изготовления, является недостаточная обеспеченность рецептурно-производственных аптек необходимыми активными фармацевтическими ингредиентами (АФИ) и современными вспомогательными веществами. Многие субстанции на территории Российской Федерации зарегистрированы в достаточно крупных фасовках, что зачастую существенно превышает потребность аптеки в данных группах веществ. Кроме того, единовременные финансовые затраты на их закупку не оправданы и экономически не целесообразны. Пути решения данного вопроса могут быть следующими: создание региональных дистрибьютеров субстанций и вспомогательных веществ, которые официально могли бы заниматься перефасовкой; регистрация дополнительных упаковок субстанций в более мелких фасовках; возможность переконтроля и продления срока годности активных субстанций и вспомогательных веществ.
Вместе с тем, использование современных вспомогательных веществ (ВВ), применяемых в промышленном производстве, актуально в экстемпоральной технологии. Такие ВВ позволят получать лекарственные формы с лучшими технологическими и потребительскими свойствами, с более длительными сроками годности и способствуют внедрению новых лекарственных форм. Однако, на данный момент в экстемпоральной практике новые ВВ используются крайне редко ввиду недостаточной осведомлённости об их существовании и технологическом назначении, а также дефицита компетенций у специалистов РПО об их применении в составе лекарственных форм. В связи с этим, стратегическим решением данного вопроса является создание совместных научно-исследовательских лабораторий на базе кафедр вузов и производственных аптек, которые позволят реализовать научное сопровождение поиска и внедрения новых рецептур и ВВ, а также разработку информационно-справочных материалов, необходимых в работе РПО. Дополнительно считаем необходимым пересмотр существующих мануальных и официнальных прописей на предмет замены ВВ и АФИ, которые устарели с позиции современной фармакологии и/или не выпускаются химико-фармацевтической промышленностью.
Разработка и применение экстемпоральных прописей требует тесного взаимодействия врача и фармацевтического работника. У современных врачей зачастую отсутствует навык выписывания экстемпоральных прописей, что ограничивает возможности врача персонифицировать подход к терапии пациента. Для решения этой проблемы предлагаем введение элективных курсов на додипломном этапе подготовки врачей, более широкое использование системы дополнительного профессионального образования в рамках непрерывного медицинского образования, проведение совместных научно-практических конференций «Врач — Провизор», позволяющих повысить информированность медицинских работников о возможностях экстемпоральной рецептуры.
Заключение / Conclusion
Лекарственные препараты экстемпорального изготовления — неотъемлемая часть персонифицированного подхода в современной медицине. При этом нормативно-правовое регулирование деятельности рецептурно-производственных отделов аптек несовершенно и требует оптимизации с участием научных и профессиональных сообществ, а также регуляторных органов и представителей бизнеса. Решение проблем, приведённых в статье, позволит вывести экстемпоральное производство на новый, более совершенный уровень и расширить возможности персонифицированной медицины.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Участие авторов
Все авторы внесли существенный вклад в подготовку работы, прочли и одобрили финальную версию статьи перед публикацией. Чикина И. В. — постановка задач исследования, концепция, написание и редактирование статьи, критический анализ нормативно-правовой базы, финальное утверждение рукописи; Онегин С. В., Парфенов А. А., Трубников А. А. — критический анализ нормативно-правовой базы, написание и редактирование статьи.
Финансирование
Работа выполнялась без спонсорской поддержки.
ADDITIONAL INFORMATION
Conflict of interests
The authors declare no conflict of interest.
Authors’ participation
All the authors made a significant contribution to the preparation of the work, read and approved the final version of the article before publication. Chikina IV — setting research objectives, concept, writing and editing the article, critical analysis of the regulatory framework, final approval of the manuscript; Onegin SV, Parfenov AA, Trubnikov AA — critical analysis of the regulatory framework, writing and editing the article.
Financing
The work was carried out without sponsorship.
Список литературы
1. Долгополов И.С., Рыков М.Ю. Персонифицированная медицина: современные тенденции и перспективы. Российский вестник перинатологии и педиатрии. 2022;67(4):14-21. https://doi.org/10.21508/1027-4065-2022-67-4-14-21.
2. Сокольская М.А., Шварц В.А., Хугаева Э.А., Бокерия О.Л. Потребность и заинтересованность пациентов с кардиохирургической патологией в дистанционном динамическом наблюдении с помощью интернет-сервисов. Здравоохранение Российской Федерации. 2021;65(3):222-229. https://doi.org/10.47470/0044-197X-2021-65-3-222-229.
3. Белялов Ф.И. Индивидуализированная медицина в клинической практике. Клиническая медицина. 2020;98(1):61-67. https://doi.org/10.34651/0023-2149-2020-98-1-61-67.
4. Наркевич И.А., Похваленко Е.В. Экстемпоральные лекарственные препараты для новорожденных. Фармация. 2013;7:27-29.
5. Король Л.А., Егорова С.Н., Кудлай Д.А., Краснюк И.И., Сологова С.С., Король В.А., Смолярчук Е.А., Садковский И.А., Мандрик М.А. Современная экстемпоральная рецептура в системе гериатрической медицины: текущие возможности и будущие задачи. Обзор литературы. Терапевтический архив. 2022;94(8):1020–1027. DOI: 10.26442/00403660.2022.08.201805.
6. Егорова С.Н., Неволина Е.В. Аптечное изготовление лекарственных форм: проблемы, требующие правового решения. Вестник Росздравнадзора. 2013;6:36-38.
7. Никулина М.А., Воронкина И.В., Пудовкина Т.В., Григорьева И.В. Проблемы производственного отдела аптеки в современных условиях. Международный журнал прикладных и фундаментальных исследований. 2016;2(2):265-269.
8. Шишова Л.И., Саканян Е.И., Шемерянкина Т.Б., Губарева О.Н. Фармакопейные требования к качеству лекарственных препаратов экстемпорального изготовления: настоящее и будущее. Химико-фармацевтический журнал. 2017;51(8):60-64. https://doi.org/10.30906/0023-1134-2017-51-8-61-64.
9. Алехин А.В., Эриванцева Т.Н., Ряженов В.В., Лысков Н.Б., Алехина Н.А., Кузнецова М.М. Новая роль экстемпорального изготовления в регулировании доступа лекарственных препаратов на рынок. Фармация и фармакология. 2023;11(2):161- 172. https://doi.org/10.19163/2307-9266-2023-11-2-161-172.
10. Смехова И.Е., Ладутько Ю.М., Калинина О.В. Экстемпоральное изготовление лекарственных препаратов: проблемы и решения. Вестник фармации. 2021;91(1):48-52. https://doi.org/10.52540/2074-9457.2021.1.48.
11. Пономарёва Е.А., Тюренков И.Н. Финансово-экономические аспекты функционирования производственных аптек. Вестник Росздравнадзора. 2011;2:25-33.
12. Федеральный закон 12.04.2010 №61-ФЗ «Об обращении лекарственных средств». Электронный ресурс. Дата обращения: 24.04.2024. URL: https://docs.cntd.ru/document/902209774?section=text.
13. Приказ МЗ от 22.05.2023 №249н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, имеющими лицензию на фармацевтическую деятельность». Дата обращения: 24.04.2024. Электронный ресурс. URL: https://docs.cntd.ru/document/1301699481?-section=text.
14. Приказ МЗ от 24.11.2021 №1094н «Об утверждении Порядка назначения лекарственных препаратов, форм рецептурных бланков на лекарственные препараты, Порядка оформления указанных бланков, их учета и хранения, форм бланков рецептов, содержащих назначение наркотических средств или психотропных веществ, Порядка их изготовления, распределения, регистрации, учета и хранения, а также Правил оформления бланков рецептов, в том числе в форме электронных документов». Дата обращения: 24.04.2024. Электронный ресурс. URL: https://docs.cntd.ru/document/727251258?section=text.
15. Приказ МЗ от 24.11.2021 №1093н «Об утверждении Правил отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на осуществление фармацевтической деятельности, медицинскими организациями, имеющими лицензию на осуществление фармацевтической деятельности, и их обособленными подразделениями (амбулаториями, фельдшерскими и фельдшерско-акушерскими пунктами, центрами (отделениями) общей врачебной (семейной) практики), расположенными в сельских поселениях, в которых отсутствуют аптечные организации, а также Правил отпуска наркотических средств и психотропных веществ, зарегистрированных в качестве лекарственных препаратов для медицинского применения, лекарственных препаратов для медицинского применения, содержащих наркотические средства и психотропные вещества в том числе Порядка отпуска аптечными организациями иммунобиологических лекарственных препаратов». Электронный ресурс. Дата обращения: 24.04.2024. URL: https://docs.cntd.ru/document/727251237?section=text.
16. Государственная фармакопея Российской Федерации XV издания. Электронный ресурс. Дата обращения: 24.04.2024. URL: https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/.
17. Приказ МЗ от 25.09.2023 №448 «Об утверждении общих фармакопейных статей и фармакопейных статей и внесении изменений в приказ Министерства здравоохранения Российской Федерации от 20.07.2023 N 377 «Об утверждении общих фармакопейных статей и фармакопейных статей». Дата обращения: 24.04.2024. Электронный ресурс. URL: https://docs.cntd.ru/document/1302604017?section=text.
18. Постановление Главного государственного санитарного врача РФ от 24.12.2020 №44 «Об утверждении санитарных правил СП 2.1.3678- 20 "Санитарно-эпидемиологические требования к эксплуатации помещений, зданий, сооружений, оборудования и транспорта, а также условиям деятельности хозяйствующих субъектов, осуществляющих продажу товаров, выполнение работ или оказание услуг». Дата обращения: 24.04.2024. Электронный ресурс. URL: https://docs.cntd.ru/document/573275590?section=text.
Об авторах
И. В. ЧикинаРоссия
Чикина Ирина Владимировна — старший преподаватель, кафедра фармакогнозии и фармацевтической технологии
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
С. В. Онегин
Россия
Онегин Сергей Владимирович — к. фарм. н., доцент, кафедра фармакогнозии и фармацевтической технологии
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. А. Парфенов
Россия
Парфенов Андрей Александрович— к. фарм. н., доцент, кафедра фармакогнозии и фармацевтической технологии
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. А. Трубников
Россия
Трубников Алексей Александрович — к. фарм. н., доцент, кафедра фармакогнозии и фармацевтической технологии
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Чикина И.В., Онегин С.В., Парфенов А.А., Трубников А.А. Современное экстемпоральное фармацевтическое производство: проблемы и перспективы. Пациентоориентированная медицина и фармация. 2024;2(2):43-50. https://doi.org/10.37489/2949-1924-0049. EDN: LCXGIU
For citation:
Chikina I.V., Onegin S.V., Parfenov A.A., Trubnikov A.A. Modern extemporaneous pharmaceutical manufacturing: problems and prospects. Patient-Oriented Medicine and Pharmacy. 2024;2(2):43-50. (In Russ.) https://doi.org/10.37489/2949-1924-0049. EDN: LCXGIU
JATS XML


































.png)
