Перейти к:
Наночастицы золота для тераностики в онкологии
https://doi.org/10.37489/2949-1924-0074
EDN: IWJYBW
Аннотация
Химическая стабильность, низкая токсичность, относительная простота методов синтеза и модификации наночастиц золота открывает широкие возможности их использования в качестве тераностических агентов для диагностики и лечения онкологических заболеваний. Уникальные свойства наночастиц золота, известные как локализованный поверхностный плазмонный резонанс, позволяют создавать на их основе тераностические агенты, сочетающие в себе возможности как диагностики in vitro, так и адресной доставки лекарств. Высокое соотношение площади поверхности к объёму наночастиц золота существенно облегчает создание на их основе комплексных наноплатформ, используемых сразу в нескольких терапевтических и диагностических направлениях.
Ключевые слова
Для цитирования:
Курапов П.Б., Бахтенко Е.Ю. Наночастицы золота для тераностики в онкологии. Пациентоориентированная медицина и фармация. 2024;2(4):100-104. https://doi.org/10.37489/2949-1924-0074. EDN: IWJYBW
For citation:
Kurapov P.B., Bakhtenko E.J. Gold nanoparticles for theranostic treatment of cancer. Patient-Oriented Medicine and Pharmacy. 2024;2(4):100-104. (In Russ.) https://doi.org/10.37489/2949-1924-0074. EDN: IWJYBW
Введение / Introduction
Традиционные лекарственные препараты после их введения распределяются по организму согласно их физико-химическим свойствам, таких, как растворимость, гидрофильность и гидрофобность, степень и ионизации и т. п. В ряде случаев для достижения активной концентрации лекарственного средства, способной вызвать стандартный терапевтический эффект, необходимы высокие и не всегда безопасные дозы препарата. Вероятность самого лекарства и реагирующих с ним молекул активного центра взаимодействовать друг с другом или проникать через клеточные мембраны существенно выше при высоких концентрациях препарата. Хорошо известно, что проникновение лекарства через различные биологические барьеры, в том числе через клеточные оболочки, или образование метаболитов замедляется по мере уменьшения концентрации действующего вещества [1][2].
Очень часто традиционные лекарственные формы не обеспечивают эффективную доставку терапевтических или диагностический препаратов внутрь целевых клеток. Для эффективного решения этой задачи, обеспечения целенаправленного транспорта лекарств и диагностикумов в орган, ткань или клетку-мишень можно с успехом использовать технологии адресной доставки с использованием наноносителей. При этом особый интерес представляет создание таких наноносителей, которые сочетают в себе возможность использования их не только как терапевтические, но и также как диагностические агенты. Такие конструкции (платформы) получили название тераностических агентов или тераностиков.
Термин тераностика, который появился сравнительно недавно, возник при сочетании двух понятий «терапия» и «диагностика». Тераностика включает в себя направление в медицине, которое основано на комплексном решении диагностических и терапевтических задач путём создания препаратов, которые одновременно являются комбинированным терапевтическим и диагностическим средством.
Материалы, для создания наноносителей для тераностики должны обладать особым комплексом физико-химических характеристик. Такие наноносители должны быть в первую очередь химически стабильны, биосовместимы, нетоксичны и иметь достаточно большую площадь поверхности, на которой можно с помощью простых манипуляций закрепить (разместить) лекарственный препарат. Однако главное требование к материалу, из которого изготовлен наноноситель, состоит в том, чтобы он обладал специфичными и уникальными свойствами для биологической визуализации или физического зондирования. Не менее важно, чтобы технологии синтеза таких наноносителей были просты, воспроизводимы и легко управляемы с помощью точной технологии, включая такие показатели как их состав, размер, морфология и химия поверхности [3].
Разумеется, создание таких наноносителей (наноплатформ) задача чрезвычайно сложная и требует всесторонних знаний и опыта как в области химии, физики, и материаловедения, так фармацевтики и биомедицины. В настоящий момент известно ограниченное число материалов, которые можно использовать для успешного конструирования таких наноконструкций для тераностики.
Научные исследования и практические разработки многих авторов по всему миру свидетельствуют о том, что одним из наиболее перспективных материалов для создания наноносителей для тераностики могут служить наночастицы золота. В настоящее время наночастицы золота в основном используются по двум направлениям. Первое связано с биомедицинскими исследованиями, диагностикой, фототермической и фотодинамической терапиями. Второе направление сконцентрировано на создании конструкций для адресной доставки лекарственных средств или генетических материалов.
Таким образом, задача, которая стоит перед создателями тераностических препаратов на основе наночастиц золота, сводится к разработке эффективных технологий, сочетающих в себе оба эти направления.
Обсуждение / Discussion
Наночастицы золота весьма перспективны для создания тераностических конструкций, так как, во-первых, имеют уникальные оптические свойства, которые обусловлены взаимодействием света с электронами на их поверхности. При определённой длине волны света колебания электронов на поверхности наночастиц вызывают локализованный поверхностный плазмонный резонанс. Это явление приводит к сильному затуханию света (поглощению и рассеянию), т. е. наночастицы золота являются чрезвычайно эффективными фотосенсибилизаторами. Конкретная длина волны света, при котором наблюдается поверхностный плазмонный резонанс, зависит от размера, формы, поверхности и состояния агломерации наночастиц золота. Такой уникальный эффект позволяет использовать наночастицы золота как контрастное вещество или как усилитель дозы при лучевой и фототермической терапии.
Оптические свойства наночастиц золота предсказуемо зависят от их размера и формы. Используя различные технологии синтеза наночастиц золота можно легко настроить поверхностный плазмонный резонанс на получение максимумов поглощения от 500 нм до ближней инфракрасной части спектра. Например, сферические наночастицы золота, полученные из коллоидных растворов, имеют максимумы поглощения в диапазоне 515–570 нм, в то время как наночастицы неправильной формы (стержни, ежи, звёзды) поглощают свет в ближней инфракрасной области. Такая разница в поглощающих свойствах наночастиц золота одинакового среднего размера сферической и неправильной формы обусловлена анизотропным (неравномерным) распределением поверхностных электронных слоёв [4–6].
Во-вторых, синтез и изготовление наночастиц золота различной формы хорошо разработаны. Такие переменные как состав, размер, форма, морфология и химия поверхности наночастиц легко контролируемы с помощью точных технологий. Наночастицы золота химически стабильны, нетоксичны и биосовместимы.
В-третьих, неоспоримым преимуществом наночастиц золота является то, что они имеют большую площадь поверхности относительно своего размера. Эта поверхность легко модифицируется различными лигандами, содержащими атомы азота, серы или фосфора и другие функциональные линкеры. Модифицированные наночастицы золота способны присоединять не только лекарственные средства, но и определённые антитела, которые можно использовать для активной диагностики.
Таким образом, наночастицы золота, обладающие уникальными физическими и химическими характеристиками, являются удобной платформой для создания тераностических агентов, сочетающих в себе диагностику и терапию (см. рис.).
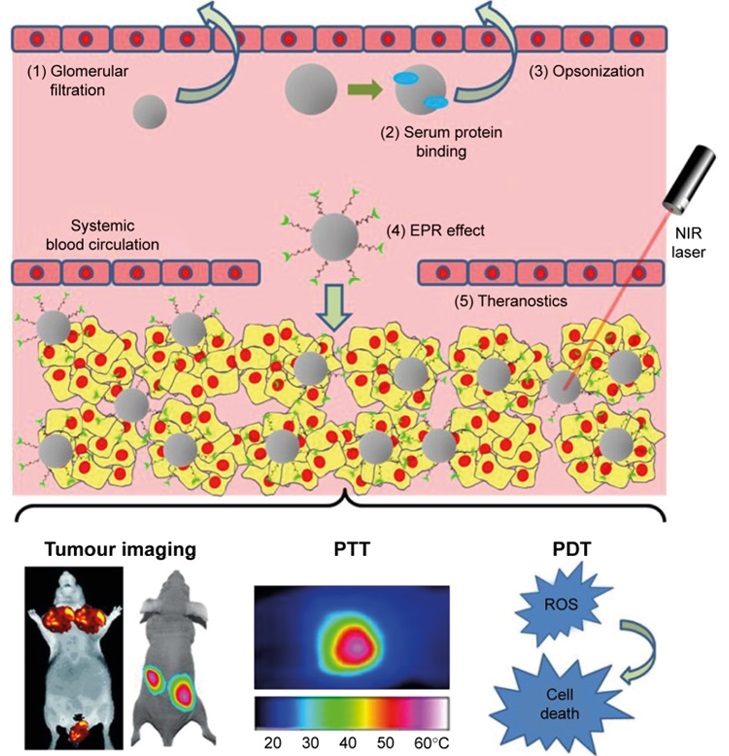
Рис. Системная доставка многофункциональных наночастиц золота для биовизуализации и фототерапии рака [7]
(1) После внутривенной инъекции небольшие наночастицы золота размером до 6 нм могут проникать через стенки кровеносных сосудов. (2-3) Белки крови могут неспецифически взаимодействовать с наночастицами золота, образуя комплексы, которые в свою очередь могут подвергаться опсонизации. (4) Более крупные биосовместимые и модифицированные по схеме лиганд-рецептор наночастицы золота (~100 нм) способны эффективно взаимодействовать и накапливаться исключительно внутри опухолевых тканей посредством «ЭПР» эффекта и специфически воздействовать на них. (5) Как результат — тераностические наночастицы золота могут не только визуализировать опухоли, но и эффективно индуцировать фототермический и фотодинамический эффекты под воздействием ближнего ИК-света.
Fig. Systemic delivery of multifunctional gold nanoparticles for biovisualization and phototherapy of cancer [7]
(1) After intravenous injection, small gold nanoparticles up to 6 nm in size can penetrate the walls of blood vessels. (2-3) Blood proteins can interact non-specifically with gold nanoparticles, forming complexes, which in turn can undergo opsonization. (4) Larger biocompatible and modified gold nanoparticles (~100 nm) according to the ligand-receptor scheme are able to effectively interact and accumulate exclusively inside tumor tissues through the "EPR" effect and specifically affect them. (5) As a result, theranostic gold nanoparticles can not only visualize tumors but also effectively induce photothermal and photodynamic effects under the influence of near-infrared light.
Наночастицы (~100 нм) с биоактивными целевыми лигандами и/или агентами биовизуализации могут эффективно накапливаться внутри опухолевых тканей посредством EPR эффекта и специфически воздействовать на раковые клетки через путь лиганд-рецептор. В результате тераностические наночастицы золота могут визуализировать опухоли за счёт плазмонного резонанса, вызванного облучение светом лазера в ближнем ИК диапазоне [8][9].
В настоящее время уже два лекарственных препарата на основе наночастиц золота Aurimmune™ и AuroLase™ с внутривенным способом введения прошли клиническую апробацию. В терапии AuroLase™ используется уникальная «оптическая настройка» нового класса наночастиц золота, которые могут преобразовывать свет в тепло для термического разрушения опухоли [10].
Заключение / Conclusion
Модифицированные и биосовместимые наночастицы золота благодаря своим уникальным свойствами являются чрезвычайно перспективными тераностическими агентами для клинической диагностики и адресной доставки лекарственных препаратов для лечения рака, болезни Альцгеймера, гепатита, туберкулёза, сахарного диабета и других заболеваний. Плазмонная фототермическая лазерная терапия раковых опухолей с помощью наночастиц золота перешла в стадию клинических испытаний.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Финансирование
Работа выполнялась без спонсорской поддержки.
Участие авторов
Все авторы внесли существенный вклад в подготовку работы, прочли и одобрили финальную версию статьи перед публикацией. Курапов П. Б. — концепция и дизайн исследования, написание текста, редактирование; Бахтенко Е. Ю. — написание текста рукописи анализ релевантных научных публикаций по теме.
ADDITIONAL INFORMATION
Conflict of interests
The authors declare no conflict of interest.
Financing
The work was carried out without sponsorship.
Authors’ participation
All authors made a significant contribution to the preparation of the work, read and approved the final version of the article before publication. Kurapov BP — research concept and design, writing, editing; Bakhtenko EJu — writing the text of the manuscript and analyzing relevant scientific publications on the topic.
Список литературы
1. Чехонин В.П., Баклаушев В.П., Кузнецов Д.А. Медицинские нанобиотехнологии адресной доставки диагностических и лекарственных препаратов. Вестник РГМУ. 2010;(3):6-10.
2. Чехонин В.П., Меркулов В.А., Кузнецов Д.А., и др. Перспективы применения нанобиотехнологий в медицине. Вестник РГМУ. 2009;(1):7- 11.
3. Курапов П.Б., Бахтенко Е.Ю. Наночастицы золота для диагностики и терапии онкологических заболеваний. Вестник РГМУ. 2018;(6):86–93. DOI: 10.24075/vrgmu.2018.090 DOI: 10.24075/brsmu.2018.090
4. Faheem SM, Hussaina Banu. Gold Nanoparticles in Cancer Diagnosis and Treatment: A Review. Austin J Biotechnol Bioeng. 2014;1(6):1-5.
5. Khan AK, Rashid R, Murtaza G, Zahra A. Gold Nanoparticles: Synthesis and Applications in Drug Delivery. Tropical Journal of Pharmaceutical Research. 2014;13(7):1169-1177. DOI:10.4314/tjpr.v13i7.23.
6. Alaqad K, Saleh TA. Gold and Silver Nanoparticles: Synthesis Methods, Characterization Routes and Applications towards Drugs. Journal of Environmental & Analytical Toxicology. 2016:384. 1-10. DOI:10.4172/2161-0525.1000384.
7. Guo J, Rahme K, He Y, Li LL, Holmes JD, O'Driscoll CM. Gold nanoparticles enlighten the future of cancer theranostics. Int J Nanomedicine. 2017 Aug 22;12:6131-6152. doi: 10.2147/IJN.S140772.
8. Bansal SA, Kumar V, Karimi J, Singh AP, Kumar S. Role of gold nanoparticles in advanced biomedical applications. Nanoscale Adv. 2020 Jul 16;2(9):3764- 3787. doi: 10.1039/d0na00472c.
9. Дыкман Л. А., Хлебцов Н. Г. Биомедицинское применение многофункциональных золотых нанокомпозитов. Успехи биологической химии. 2016;56:411–450.
10. Perry HL, Botnar RM, Wilton-Ely JDET. Gold nanomaterials functionalised with gadolinium chelates and their application in multimodal imaging and therapy. Chem Commun (Camb). 2020 Apr 14;56(29):4037-4046. doi: 10.1039/d0cc00196a.
Об авторах
П. Б. КураповРоссия
Курапов Павел Борисович — д. б. н., доцент, профессор кафедры медицинских нанобиотехнологий
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Е. Ю. Бахтенко
Россия
Бахтенко Елена Юрьевна — д. б. н., доцент, директор филиала
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Курапов П.Б., Бахтенко Е.Ю. Наночастицы золота для тераностики в онкологии. Пациентоориентированная медицина и фармация. 2024;2(4):100-104. https://doi.org/10.37489/2949-1924-0074. EDN: IWJYBW
For citation:
Kurapov P.B., Bakhtenko E.J. Gold nanoparticles for theranostic treatment of cancer. Patient-Oriented Medicine and Pharmacy. 2024;2(4):100-104. (In Russ.) https://doi.org/10.37489/2949-1924-0074. EDN: IWJYBW
JATS XML


































.png)
