Перейти к:
Анализ процессов регистрации и производства препаратов группы гепарина в России
https://doi.org/10.37489/2949-1924-0071
EDN: PUVPZV
Аннотация
Цель. Провести анализ процессов обращения лекарственных препаратов группы гепарина за 2004–2024 гг. с точки зрения темпов регистрации и локализации производства активной фармацевтической субстанции (АФС), готовой лекарственной формы (ГЛФ), перспектив осуществления полного производственного цикла на территории Российской Федерации.
Материалы и методы. Проведён анализ сведений 693 реестровых записей, размещённых в Государственном реестре лекарственных средств (ГРЛС) и посвящённых препаратам группы гепарина, собрана база данных в Microsoft Excel. Информация о зарегистрированных лекарственных препаратах была классифицирована в соответствии с принадлежностью к группе гепарина, наименованию действующего вещества, лекарственной форме, дате регистрации, наличию в перечне жизненно необходимых и важнейших лекарственных препаратов, стране производства АФС и ГЛФ.
Результаты. В соответствии с анатомо-терапевтическо-химической классификацией к препаратам группы гепарина были отнесены препараты более 20 наименований: препараты нефракционированного гепарина, низкомолекулярных фракций гепарина, гепариноидов и антитромбина III. Изучено 95 действующих регистрационных удостоверения (РУ) и 13 РУ, исключённых из ГРЛС, — всего 108 РУ. Построены графики, отражающие темпы регистрации лекарственных препаратов (ЛП) заявленной группы. Наибольшие темпы регистрации наблюдаются в период времени с 2020 по 2024 гг. — в среднем ежегодно получают регистрационное удостоверение 5,25 лекарственных препарата. Годы наиболее активной регистрации — 2011 (11 одобренных ЛП), 2017 (8 одобренных ЛП) и 2023 год (9 одобренных ЛП). Локализация производства препаратов группы гепарина на 2024 год представлена на диаграммах. Основной страной производства АФС гепарина натрия является Китай. Однако для каждого пятого препарата группы гепарина существует возможность проведения полного производственного цикла на территории России, включая синтез АФС.
Выводы. Получены сведения о структуре ассортимента (95 ЛП представлены в 10 лекарственных формах для различных 5 путей введения), темпах регистрации препаратов группы гепарина и локализации производства АФС, готовой лекарственной формы. Локализация производства АФС гепарина натрия сосредоточена в Китае. Известны сведения о строительстве в ближайшие годы в России трёх производственных площадок по производству АФС гепарина натрия: китайской компанией «Хэбэй Чаншань Биокемикал Фармасьютикал Ко. Лтд», российскими компаниями ООО «Фармасинтез-Кама» и ООО «Северный океан». На момент исследования число препаратов, для которых поставщиком АФС заявлены только российские компании — 3 лекарственных препарата. Производство ГЛФ препаратов в значительной степени локализовано в России (75,4 % для препаратов гепарина натрия и 65,1 % для препаратов низкомолекулярных фракций гепарина).
Ключевые слова
Для цитирования:
Лаврентьева Л.И., Захаров А.В. Анализ процессов регистрации и производства препаратов группы гепарина в России. Пациентоориентированная медицина и фармация. 2024;2(4):74-81. https://doi.org/10.37489/2949-1924-0071. EDN: PUVPZV
For citation:
Lavrentyeva L.I., Zakharov A.V. Analysis of the registration and manufacturing of heparin drugs in Russia. Patient-Oriented Medicine and Pharmacy. 2024;2(4):74-81. (In Russ.) https://doi.org/10.37489/2949-1924-0071. EDN: PUVPZV
Введение / Introduction
В соответствии с анатомо-терапевтическо-химическим классификатором к группе гепарина (код АТХ: B01AB) были отнесены препараты гепарина натрия, препараты низкомолекулярных фракций гепарина, гепариноидов и препараты гликопротеина антитромбин III [1]. В соответствии с Решением Совета Евразийской экономической комиссии № 89 все названные группы препаратов относятся к биологическим препаратам: гепарины являются гликозамингликанами, а антитромбин III — гликопротеином [2].
Монопрепараты гепарина натрия, зарегистрированные в лекарственных формах системного действия показаны для терапии и профилактики тромбоэмболических осложнений и тромбозов, терапии нарушений микроциркуляции (в том числе при гемолитико-уремическом синдроме), профилактике свёртывания крови при гемодиализе и применяются для обработки периферических венозных катетеров.
Монопрепараты и комбинированные препараты гепарина натрия, зарегистрированные в лекарственных формах местного действия, применяются для терапии ушибов и травм, гематом, отёков мягких тканей, при остром и хроническом геморрое.
Препараты низкомолекулярных фракций гепарина и гепариноиды применяются при профилактике и терапии тромбоэмболий, тромбозов (в том числе тромбозе глубоких вен), профилактике свёртывания крови при гемодиализе.
Препараты антитромбина III применяются для профилактики и терапии тромбозов и тромбоэмболий.
Монопрепараты гепарина натрия системного действия, препараты эноксапарина натрия, парнапарина натрия включены в перечень жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) [3].
Для препаратов группы гепарина характерны внутривенный и подкожный пути введения, наружное применение, за исключением препаратов гепариноида сулодексида — для препаратов сулодексида доступны пероральный путь введения (используется лекарственная форма капсулы) и внутримышечный путь введения.
Изучение процессов регистрации и локализации производства гепаринов в России является важным аспектом обеспечения доступности эффективных ЛП для пациентов.
Цель исследования / Objective
Провести анализ процессов обращения лекарственных препаратов группы гепарина за 2004–2024 гг. с точки зрения темпов регистрации, в том числе по процедуре Евразийского экономического союза (ЕАЭС), и локализации производства активной фармацевтической субстанции (АФС), готовой лекарственной формы (ГЛФ).
Материалы и методы / Materials and methods
Для проведения исследования была собрана база данных в Microsoft Excel по результатам анализа 693 реестровых записей, размещённых в Государственном реестре лекарственных средств [4]. В анализ вошла история изменений и актуальные данные 95 действующих регистрационных удостоверений, 13 регистрационных удостоверений с истёкшим сроком действия, — всего 108 регистрационных удостоверения.
Полученные сведения представлены в виде столбчатых диаграмм, отражающих темпы регистрации (рис. 1–4), круговых диаграмм, отражающих локализацию производства АФС и ГЛФ (рис. 5–8) и обсуждены в тексте статьи.
Результаты и обсуждение / Results and discussion
Группа гепарина (код АТХ: B01AB) была разделена на 4 подгруппы, в зависимости от действующих веществ:
- монопрепараты нефракционированного гепарина;
- комбинированные препараты нефракционированного гепарина;
- препараты низкомолекулярных фракций гепарина и гепариноидов;
- препараты антитромбина III.
Для каждого международного непатентованного наименования и группировочного наименования приведены сведения о числе зарегистрированных препаратов, доступных лекарственных формах, наличии в перечне ЖНВЛП и сведения о числе препаратов, зарегистрированных в соответствии с процедурой ЕАЭС.
Препараты группы гепарина, не получившие регистрации в РФ на 2024 год — ревипарин натрия, данапароид натрия, тинзапарин натрия.
Наибольшее число лекарственных препаратов, имеющих регистрацию по процедуре ЕАЭС — препараты эноксапарина натрия (9 ЛП), надропарина натрия (7 ЛП), гепарина натрия — системного действия (7 ЛП), гепарина натрия — местного действия (5 ЛП), далтепарина натрия (5 ЛП) и препараты бензилникотината + бензокаина + гепарина натрия (5 ЛП) — см. таблицу.
Таблица. Регистрация лекарственных препаратов группы гепарина в Российской Федерации в 2024 году
Table. Registration of heparin drugs in the Russian Federation in 2024
Наименование [1] | Число зарегистрированных ЛП на 2024 год / Разработанная лекарственная форма [4] | Наличие в перечне ЖНВЛП [3] | Доля ЛП, имеющих регистрацию по требованиям ЕАЭС |
Монопрепараты нефракционированного гепарина | |||
Гепарин натрия | 3 / раствор для инъекций 14 / раствор для внутривенного и подкожного введения | Да | 7 из 17 (41 %) |
Гепарин натрия | 15 / гель для наружного применения | Нет | 5 из 15 (33 %) |
Комбинированные препараты нефракционированного гепарина | |||
Гепарин натрия + Декспантенол + | 7 / гель для наружного применения | Нет | 5 из 7 (71 %) |
Гепарин натрия + Фосфолипиды + Эсцин | 1 / гель для наружного применения | Нет | 1 из 1 (100 %) |
Гепарин натрия + Декспантенол + Троксерутин | 2 / гель для наружного применения | Нет | 2 из 2 (100 %) |
Гепарин натрия + Декспантенол + Троксерутин + Бензокаин | 0* / гель для наружного применения | Нет | н/п |
Бензилникотинат + Бензокаин + Гепарин натрия | 6 / мазь для наружного применения | Нет | 5 из 6 (83 %) |
Мометазон + Гепарин натрия | 0** / крем для наружного применения | Нет | н/п |
Гепарин натрия + Аллантоин + Декспантенол | 0*** / крем для наружного применения | Нет | н/п |
Гепарин натрия + Лауромакрогол 400 + Преднизолон | 1 / суппозитории ректальные 2 / мазь для ректального и наружного применения | Нет | 2 из 3 (66 %) |
Бензокаин + Гепарин натрия | 3 / суппозитории ректальные | Нет | 2 из 3 (66 %) |
Гепарин натрия + Лидокаин + Преднизолон | 1 / суппозитории ректальные | Нет | 1 из 1 (100 %) |
Препараты низкомолекулярных гепаринов и гепариноидов | |||
Далтепарин натрия | 7 / раствор для внутривенного и подкожного введения | Нет | 5 из 7 (71 %) |
Эноксапарин натрия | 12 / раствор для инъекций | Да | 9 из 12 (75 %) |
Надропарин кальция | 7 / раствор для подкожного введения 5 / раствор для инъекций | Нет | 7 из 12 (58 %) |
Парнапарин натрия | 1 / раствор для подкожного введения | Да | 0 из 1 (0 %) |
Ревипарин натрия | ЛП ранее не зарегистрированы в России | н/п | н/п |
Данапароид натрия | ЛП ранее не зарегистрированы в России | н/п | н/п |
Тинзапарин натрия | ЛП ранее не зарегистрированы в России | н/п | н/п |
Сулодексид | 2 / капсулы 3 / раствор для внутривенного и внутримышечного введения | Нет | 1 из 5 (20 %) |
Бемипарин натрия | 2 / раствор для инъекций | Нет | 0 из 2 (0 %) |
Препараты антитромбина III | |||
Антитромбин III | 1 / лиофилизат для приготовления раствора для инфузий | Нет | 1 из 1 (100 %) |
Примечания: * — Лекарственный препарат Тромблесс® Плюс был зарегистрирован в России в период с 07.2012 по 06.2024 гг.
** — Лекарственный препарат Скинлайт был зарегистрирован в России в период с 10.2011 по 02.2022 гг.
*** — Лекарственный препарат Гепатромбин в 4 дозировках был зарегистрирован в России в период с 10.2011 по 09.2022 гг.
Notes: * — The medicinal product Trombless® Plus was registered in Russia in the period from 07.2012 to 06.2024.
** — The drug Skinlight was registered in Russia in the period from 10.2011 to 02.2022.
*** — The drug Hepatrombin in 4 dosages was registered in Russia in the period from 10.2011 to 09.2022.
Для следующих наименований действующих веществ не зарегистрировано лекарственных препаратов по процедуре ЕАЭС: парнапарин натрия (входит в перечень ЖНВЛП), бемипарин натрия.
На рис. 1–4 приведены столбчатые диаграммы отражающие темпы регистрации препаратов группы гепарина в целом (рис. 1), монопрепаратов нефракционированного гепарина (рис. 2), комбинированных препаратов нефракционированного гепарина (рис. 3) и препаратов низкомолекулярных гепаринов и гепариноидов (рис. 4).
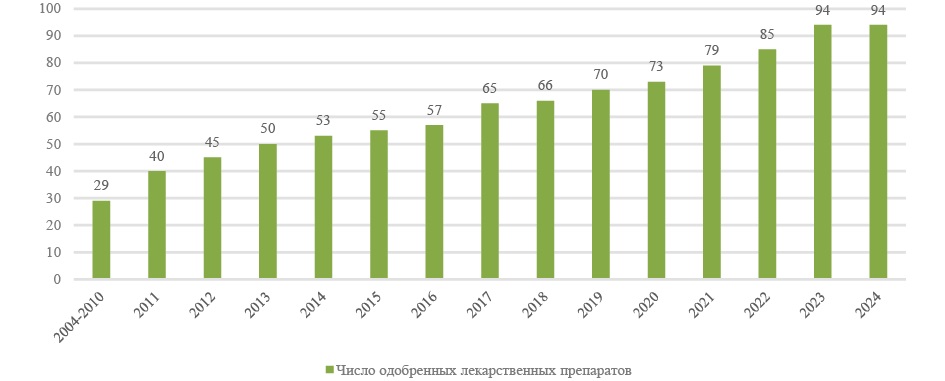
Рис. 1. Динамика регистрации всех препаратов группы гепарина (код АТХ: B01AB)
Fig. 1. Dynamics of registration of all drugs of the heparin group (ATC code: B01AB)
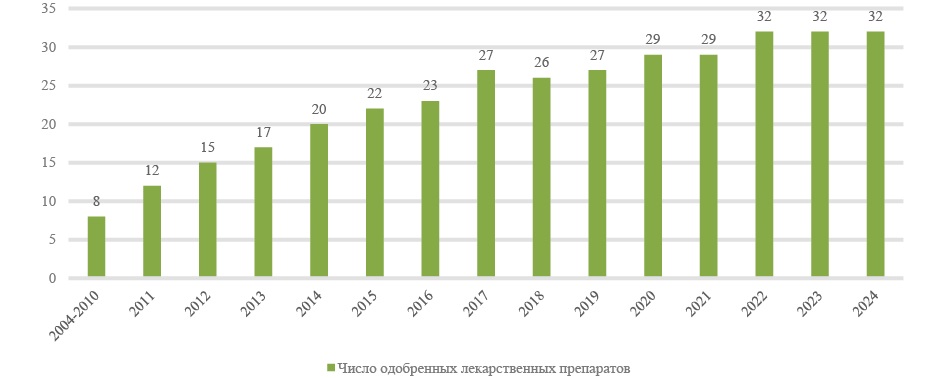
Рис. 2. Динамика регистрации монопрепаратов нефракционированного гепарина
Fig. 2. Dynamics of registration of monodrugs of unfractionated heparin
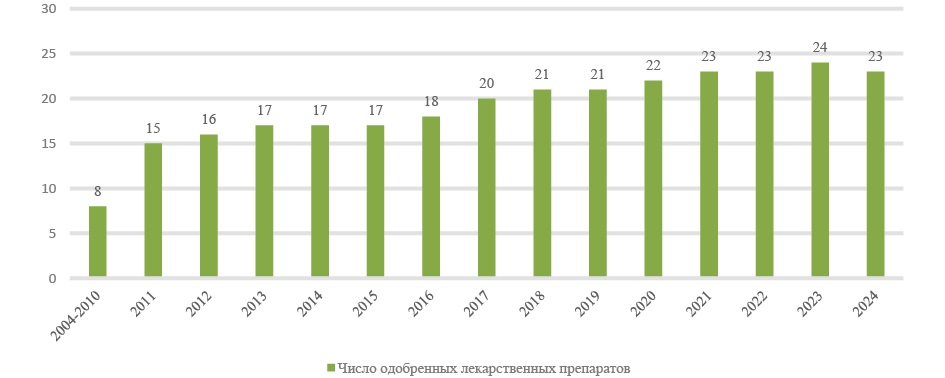
Рис. 3. Динамика регистрации комбинированных препаратов нефракционированного гепарина
Fig. 3. Dynamics of registration of combined drugs of unfractionated heparin
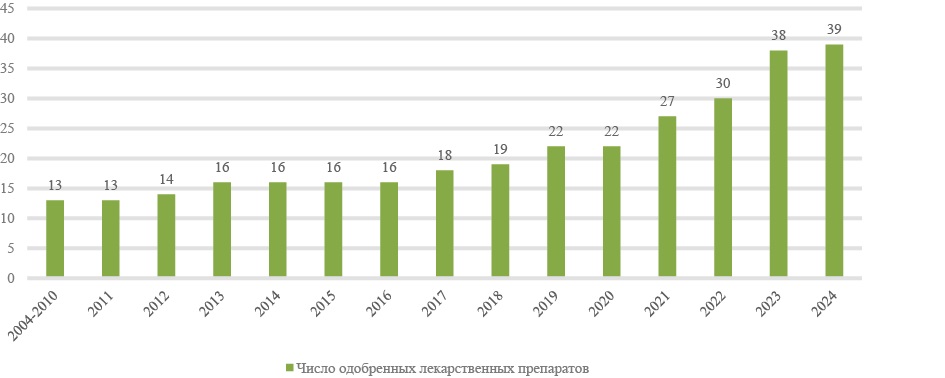
Рис. 4. Динамика регистрации препаратов низкомолекулярных гепаринов и гепариноидов
Fig. 4. Dynamics of registration of low-molecular-weight heparin and heparinoid drugs
Годы наиболее активной регистрации всех препаратов группы B01AB — 2011 (11 одобренных ЛП), 2017 (8 одобренных ЛП) и 2023 год (9 одобренных ЛП).
В 2011 году высокие темпы регистрации были обеспечены комбинированными препаратами нефракционированного гепарина в местных лекарственных формах для терапии ушибов, травм и геморроя, в 2017 году — монопрепаратов гепарина натрия для профилактики и терапии тромбозов и тромбоэмболических осложнений, в 2023 году наиболее высокие темпы регистрации наблюдались в группе препаратов низкомолекулярных фракций гепарина и гепариноидов.
Среднегодовые темпы регистрации препаратов группы гепарина были оценены за следующие пятилетние периоды времени и составили в абсолютных значениях (число одобренных лекарственных препаратов):
- с 2012 по 2016 гг. — 3 ЛП;
- с 2016 по 2020 гг. — 4 ЛП;
- с 2020 по 2024 гг. — 5,25 ЛП.
Наибольшие темпы регистрации наблюдаются в период времени с 2020 по 2024 гг. — в среднем за год одобряется 5,25 лекарственных препарата.
Для оценки локализации производства АФС были изучены сведения 95 действующих регистрационных удостоверений. Локализация производства АФС гепарина натрия сосредоточена в Китае: более 70 % АФС гепарин натрия синтезируется в Китае и более 40 % — АФС низкомолекулярных гепаринов.
Известны сведения о строительстве в ближайшие годы в России трёх производственных площадок по производству АФС гепарина натрия: китайской компанией «Хэбэй Чаншань Биокемикал Фармасьютикал Ко. Лтд» в Республике Башкирия [5], российскими компаниями ООО «Фармасинтез-Коми» в Республике Татарстан (г. Набережные Челны) [6] и ООО «Северный океан» в Подмосковье (г. Воскресенск) [7].
На рис. 5–6 приведена структура локализации производства АФС «гепарин натрия».
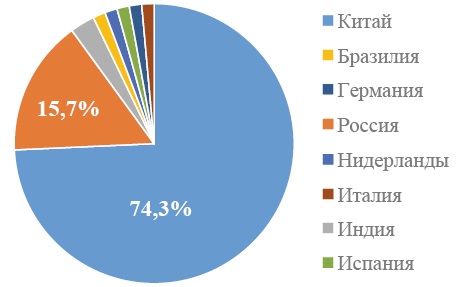
Рис. 5. Анализ локализации производства активной фармацевтической субстанции препаратов нефракционированного гепарина
Fig. 5. Analysis of the localization of production of the active pharmaceutical substance of unfractionated heparins
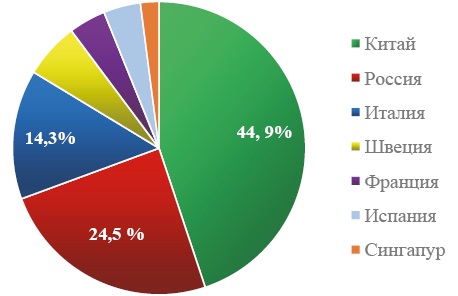
Рис. 6. Анализ локализации производства активной фармацевтической субстанции препаратов низкомолекулярных фракций гепарина и гепариноидов
Fig. 6. Analysis of the localization of production of the active pharmaceutical substance of low-molecular-weight heparin and heparinoids
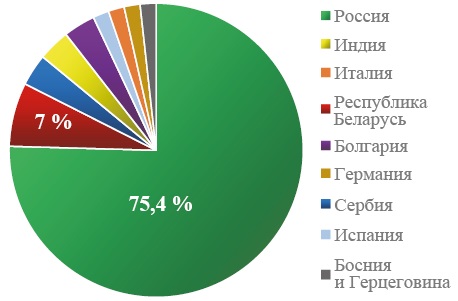
Рис. 7. Локализация производства готовой лекарственной формы препаратов нефракционированного гепарина
Fig. 7. Localization of production of finished dosage forms of unfractionated heparins
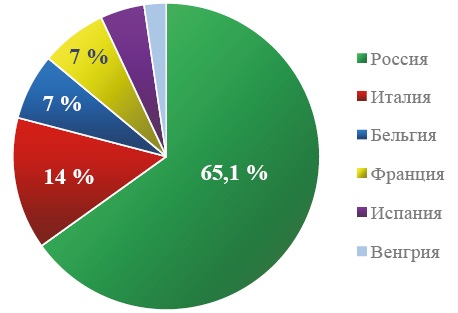
Рис. 8. Локализация производства готовой лекарственной формы препаратов гепариноидов и низкомолекулярных фракций гепарина
Fig. 8. Localization of production of finished dosage forms of heparinoids and low-molecular-weight heparin
Для производства дополнительных компонентов комбинированных препаратов гепарина используются производственные площадки следующих стран:
- бензилникотинат — Россия, Индия;
- бензокаин — Россия, Китай;
- декспантенол — Россия, Великобритания, Германия;
- диметилсульфоксид — Россия, США;
- преднизолон — Россия, Китай, Франция;
- лауромакрогол 400 — Россия, Швейцария;
- фосфолипиды — Германия;
- эсцин — Италия;
- троксерутин — Китай, Чехия, Франция;
- лидокаин — Индия.
Для оценки локализации производства готовой лекарственной формы учитывались следующие процессы: производство ГЛФ, производство ГЛФ и растворителя и осуществление всех стадий производства.
Процессы выпускающего контроля качества, упаковки, фасовки не учитывались для оценки локализации производства в данном исследовании.
Среди лидеров по производству ГЛФ препаратов группы гепарина — российские компании (75,4 % всех зарегистрированных препаратов гепарина производится в России и 65,1 % всех зарегистрированных препаратов низкомолекулярных фракций гепарина).
Производство АФС единственного зарегистрированного в России препарата антитромбина III реализуется в Австрии, ГЛФ — в Австрии и Германии.
Возможность проведения полного цикла производства возможна на территории России для 20 лекарственных препаратов группы гепарина из 95 (21 %), в основном таким образом производят препараты низкомолекулярных фракций гепарина (13 наименований препаратов из 20) следующих наименований — надропарин кальция (5 наименований), эноксапарин натрия (4 наименования) и далтепарин натрия (4 наименования).
Заключение / Conclusion
Получены сведения о темпах регистрации препаратов группы гепарина в абсолютных значениях за следующие пятилетние периоды времени: 2012 по 2016 гг. — 3 ЛП; 2016 по 2020 гг. — 4 ЛП; 2020 по 2024 гг. — 5,25 ЛП.
Годы наиболее активной регистрации — 2011 (11 одобренных ЛП), 2017 (8 одобренных ЛП) и 2023 год (9 одобренных ЛП).
В 2011 году высокие темпы регистрации были обеспечены комбинированными препаратами нефракционированного гепарина в местных лекарственных формах, в 2017 году — монопрепаратов гепарина натрия, в 2023 году — препаратами низкомолекулярных фракций гепарина и гепариноидов.
Локализация производства АФС гепарина натрия сосредоточена в Китае: более 70 % АФС гепарин натрия синтезируется в Китае и более 40 % — АФС низкомолекулярных гепаринов.
Число препаратов, для которых поставщиком АФС заявлены только российские компании — 3 из 95. На текущий момент известно о строительстве трёх производственных площадок по производству АФС гепарина на территории России.
Установлено, что для каждого пятого препарата группы гепарина существует возможность проведения полного производственного цикла на территории России. Производство ГЛФ препаратов группы гепарина в значительной степени локализовано в России (74,3 % для препаратов гепарина натрия и 44,9 % для препаратов низкомолекулярных фракций гепарина).
Таким образом, анализ процессов регистрации и производства ЛП группы гепарина в России за последние 20 лет позволил выявить ключевые тенденции, влияющие на доступность данных лекарственных препаратов для пациентов.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Финансирование
Работа выполнялась без спонсорской поддержки.
Участие авторов
Все авторы внесли существенный вклад в подготовку работы, прочли и одобрили финальную версию статьи перед публикацией.
ADDITIONAL INFORMATION
Conflict of interests
The authors declare no conflict of interest.
Financing
The work was carried out without sponsorship.
Authors’ participation
All the authors made a significant contribution to the preparation of the work, read and approved the final version of the article before publication.
Список литературы
1. ATC/DDD Index 2024 (Norwegian Institute of Public Health WHO Collaborating Centre for Drug Statistics Methodology). Режим доступа: https://atcddd.fhi.no/atc_ddd_index/.
2. Решение Совета Евразийской экономической комиссии № 89 от 03.11.2016 «Об утверждении Правил проведения исследований биологических лекарственных средств Евразийского экономического союза» Режим доступа: https://docs.eaeunion.org/docs/ru-ru/01411954/cncd_21112016_89
3. Распоряжение Правительства РФ от 12.10.2019 N 2406-р «Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи» (ред. от 16.04.2024 г.) Режим доступа: https://www.consultant.ru/document/cons_doc_LAW_335635/
4. Государственный реестр лекарственных средств. Режим доступа: https://grls.minzdrav.gov.ru/default.aspx
5. GxP news: «Китайская фармкомпания планирует запустить производство гепарина в Башкирии». Режим доступа: https://gxpnews.net/2023/04/kitajskayafarm-kompaniya-planiruet-zapustit-proizvodstvo-geparina-v-bashkirii/
6. GxP news: «Фармасинтез построит завод по выпуску фармсубстанции гепарина в Татарстане». Режим доступа: https://gxpnews.net/2024/10/farmasintez-postroit-zavod-po-vypusku-farmsubstanczii-geparina-v-tatarstane/
7. GxP news: «Производство фармсубстанции гепарина натрия в Подмосковье начнется в 2024 году». Режим доступа: https://gxpnews.net/2023/06/proizvodstvo-farmsubstanczii-geparina-natriya-v-podmoskovenachnetsya-v-2024-godu/
Об авторах
Л. И. ЛаврентьеваРоссия
Лаврентьева Лариса Ивановна — д. фарм. н., профессор, зав. кафедрой управления и экономики фармации; директор Института фармации
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. В. Захаров
Россия
Захаров Антон Валерьевич — аспирант кафедры управления и экономики фармации
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Лаврентьева Л.И., Захаров А.В. Анализ процессов регистрации и производства препаратов группы гепарина в России. Пациентоориентированная медицина и фармация. 2024;2(4):74-81. https://doi.org/10.37489/2949-1924-0071. EDN: PUVPZV
For citation:
Lavrentyeva L.I., Zakharov A.V. Analysis of the registration and manufacturing of heparin drugs in Russia. Patient-Oriented Medicine and Pharmacy. 2024;2(4):74-81. (In Russ.) https://doi.org/10.37489/2949-1924-0071. EDN: PUVPZV
JATS XML


































.png)
